题目内容
NA为阿佛伽德罗常数,下列说法正确的是( )
| A、1L1.0mol?L-1的NaAlO2的水溶液中含氧原子个数为2NA |
| B、12g石墨烯(单层石墨)中含有六元环个数为0.5NA |
| C、25℃时pH=13的NaOH溶液中含有的0H-数目为0.1NA |
| D、0.1mol基和0.1mol氢氧根离子所含电子数均为0.9NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.水分子中也含有氧原子;
B.一个六元碳环中含有1×
×6=2个C结合石墨的物质的量计算;
C.没指明溶液的体积,无法计算;
D.羟基中含有9个电子,氢氧根离子中含有10个电子.
B.一个六元碳环中含有1×
| 1 |
| 3 |
C.没指明溶液的体积,无法计算;
D.羟基中含有9个电子,氢氧根离子中含有10个电子.
解答:
解:A.水分子中也含有氧原子,所以1L1.0mol?L-1的NaAlO2的水溶液中含氧原子个数大于2NA,故A错误;
B.12g单层石墨的物质的量为1mol,一个六元碳环中含有1×
×6=2个C,所以12g单层石墨中含有六元环的个数为0.5NA,故B正确;
C.缺少溶液的体积,无法计算,故C错误;
D.0.1mol羟基中含有0.9mol电子,0.1mol氢氧根离子中含有1mol电子,二者含有的电子数不同,故D错误;
故选B.
B.12g单层石墨的物质的量为1mol,一个六元碳环中含有1×
| 1 |
| 3 |
C.缺少溶液的体积,无法计算,故C错误;
D.0.1mol羟基中含有0.9mol电子,0.1mol氢氧根离子中含有1mol电子,二者含有的电子数不同,故D错误;
故选B.
点评:本题考查物质的量的简单计算,题目难度不大,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意明确羟基与氢氧根离子的区别.

练习册系列答案
相关题目
如图甲池和乙池中的四个电极都是铂电极,乙池为K1溶液.请根据图示判断下列有关说法正确的是( )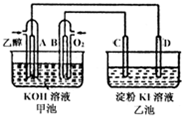

| A、甲池是电解池,乙池是原电池 |
| B、原电池的正极反应式为:C2H5OH+16OH-+12e-=2CO32-+11H2O |
| C、反应一段时间后,两池溶液的pH均未变化 |
| D、反应一段时间后,C极附近溶液变蓝 |
下列关于物质的量浓度表述正确的是( )
| A、0.3mol?L-1Na2SO4溶液中含有Na+和SO42-总物质的量为0.9mol |
| B、当1L水吸收22.4L(标准状况)氨气时所得氨水的浓度是1mol?L-1 |
| C、在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量浓度相等,则K+和Cl-的物质的量浓度一定相同 |
| D、10℃的0.35mol?L-1的KCl饱和溶液100mL,蒸发掉5g水,冷却到10℃时过滤,其滤液中溶质的物质的量浓度仍为0.35mol?L-1 |
化学与生活密切相关.下列生活中常见物质的俗名或名称与化学式相对应的是( )
| A、小苏打--Na2CO3 |
| B、烧碱--NaOH |
| C、甲醛--CH3OH |
| D、明矾--KAl(SO4)2 |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、CO和N2互为等电子体,常温常压下,22.4L的CO与1monN2所含的电子数相等 |
| B、7.8gNa2S和Na2O2的混合物中含有的阴离子数大于0.1N |
| C、1.0L0.1mol/L的醋酸溶液中含CH3COOH、CH3COO-粒子总数为0.1NA |
| D、5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
下列离子方程式正确的是( )
| A、向100mL 0.1mol/L的FeSO4溶液中,加入0.01mol Na2O2固体2Fe2++2Na2O2+2H2O═4Na++2Fe(OH)2+O2↑ |
| B、向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
| C、在硫酸工业中,对尾气中的SO2用过量的氨水吸收的反应:NH3?H2O+SO2=NH4++HSO3- |
| D、向20mL 0.5mol/L FeBr2溶液中通入448mL Cl2(标准状况)2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2. |
吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”.中国科学家尝试用Na2SeO3清除人体内的活性氧,Na2SeO3的作用是( )
| A、还原剂 |
| B、氧化剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |