题目内容
由两种金属组成的合金50g与氯气完全反应后,得到121g产物,则该合金的可能组成是( )
| A、Na、Zn |
| B、Na、Al |
| C、Fe、Mg |
| D、Zn、Cu |
考点:有关混合物反应的计算
专题:计算题
分析:两种金属组成的合金50g与氯气完全反应后,得121g产物,故参加反应的氯气为121g-50g=71g,物质的量为1mol,假设金属都为+2价,据此计算金属混合物的平衡相对原子质量,利用平均值法判断.
解答:
解:两种金属组成的合金50g与氯气完全反应后,得121g产物,故参加反应的氯气为121g-50g=71g,物质的量为
=1mol,假设金属都为+2价,则金属混合物的平均相对原子质量为
=50,
A.若Na为+2价,则其相对原子质量为46,Zn的相对原子质量为65,二者平均相对分子质量介于46~65之间,可为50,故A正确;
B.若Na为+2价,则其相对原子质量为46,当Al的化合价为+2价时,可看成其相对原子质量为
×27=18,二者相对分子质量都小于50,故B错误;
C.Fe与氯气反应生成FeCl3,当Fe的化合价为+2价时,可看成其相对原子质量为
×56=37.3,Mg的相对原子质量为24,二者相对分子质量都小于50,故C错误;
D.Zn的相对原子质量为65,Cu的相对分子质量为64,二者相对分子质量都大于50,故D错误.
故选A.
| 71g |
| 71g/mol |
| 50 |
| 1 |
A.若Na为+2价,则其相对原子质量为46,Zn的相对原子质量为65,二者平均相对分子质量介于46~65之间,可为50,故A正确;
B.若Na为+2价,则其相对原子质量为46,当Al的化合价为+2价时,可看成其相对原子质量为
| 2 |
| 3 |
C.Fe与氯气反应生成FeCl3,当Fe的化合价为+2价时,可看成其相对原子质量为
| 2 |
| 3 |
D.Zn的相对原子质量为65,Cu的相对分子质量为64,二者相对分子质量都大于50,故D错误.
故选A.
点评:本题考查混合物的计算,难度中等,本题利用平均值法解答,注意化合价与相对原子质量的转化以及金属在反应中表现的化合价.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
在相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法正确的是( )
| A、CO2和SO2中物质的量比为 1:1 |
| B、CO2和SO2的密度比为1:1 |
| C、CO2和SO2的物质的量浓度比为11:16 |
| D、CO2和SO2中所含氧原子个数比为1:1 |
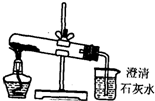 设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,难以达到预期目的是( )
设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,难以达到预期目的是( )| A、分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢 |
| B、分别将等量的白色粉末配成溶液,然后加入BaCl2溶液,看是否有沉淀生成 |
| C、分别将等量的白色粉末配成溶液,然后加入澄清石灰水,看是否有沉淀生成 |
| D、分别将等量的白色粉末用图中装置进行实验,比较澄清石灰水是否变混浊 |
将氯化钠、乙醇、碘分别从以下三组混合物中分离出来:①氯化钠和水 ②乙醇和水 ③碘和水,宜采取的操作方法依次是( )
| A、蒸发、蒸馏、萃取 |
| B、萃取、蒸馏、蒸发 |
| C、蒸发、萃取、蒸馏 |
| D、蒸馏、萃取、蒸发 |
配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因是( )
| A、容量瓶中原有少量蒸馏水 |
| B、称量药品时间过长 |
| C、定容时俯视液面 |
| D、洗涤烧杯和玻棒的溶液转入容量瓶中 |
 一定温度下,在2L的密闭容器中发生反应:A(g)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图.下列有关说法不正确的是( )
一定温度下,在2L的密闭容器中发生反应:A(g)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图.下列有关说法不正确的是( )| A、x=2 |
| B、反应开始2 min内,v(B)=0.1 mol?L-1?min-1 |
| C、2 min后,降低温度平衡向右移动 |
| D、使用催化剂可以加快反应速率,但B的转化率不变 |