题目内容
11.请结合必要的方程式,尝试从微粒的电荷情况和电离平衡的移动两方面解释为什么碳酸的分步电离一步比一步困难?(请用方程式并结合必要的文字来回答该小题)H2CO3≒HCO3-+H+,HCO3-≒CO32-+H+,第一步电离产生的H+对第二步电离有抑制作用,第一步电离后生成的负离子较难再进一步电离出带正电荷的氢离子.分析 多元弱酸每一步都电离出氢离子,第一步电离出的氢离子对后边的电离起抑制作用.
解答 解:多元弱酸每一步都电离出氢离子,第一步电离出的氢离子对后边的电离起抑制作用,且从带负电荷的阴离子中电离出带正电荷的阳离子更加困难,所以其电离程度越来越小,H2CO3≒HCO3-+H+,HCO3-≒CO32-+H+,第一步电离产生的H+对第二步电离有抑制作用,第一步电离后生成的负离子较难再进一步电离出带正电荷的氢离子,
故答案为:H2CO3≒HCO3-+H+,HCO3-≒CO32-+H+,第一步电离产生的H+对第二步电离有抑制作用,第一步电离后生成的负离子较难再进一步电离出带正电荷的氢离子.
点评 本题考查了弱电解质的电离以及影响弱电解质电离平衡移动的因素,题目难度不大.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
2.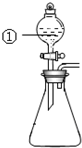 用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
 用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )| 选项 | ①中物质 | 锥形瓶中物质 | 预测锥形瓶中的现象 |
| A | 浓盐酸 | “84”消毒液 | 有黄绿色气体产生 |
| B | 浓硝酸 | 光洁的铁钉 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 先有白色沉淀生成, 后沉淀又溶解 |
| D | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色, 有黑色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有机物分子中,存在顺反异构的是( )
| A. | 2,3二溴丙烯 | B. | 2,3二甲基-2-丁烯 | ||
| C. | 丙烯 | D. | 2-丁烯 |
6.下列化学用语表述不正确的是( )
| A. | 水解方程式 HCO${\;}_{3}^{-}$+H2O═H2CO3+H3O+ | |
| B. | 水的电离 2H20?H3O++OH- | |
| C. | 醋酸的电离方程式CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 水解方程式 HCO${\;}_{3}^{-}$+H2O?H2CO3+OH- |
3.下列物质在水溶液中的电离方程式不正确的是:( )
| A. | Ca(OH)2═Ca2++2OH - | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | NH4Cl═NH3+H++Cl- | D. | HNO3═H++NO3- |
20.下列实验操作不可以实现实验目的是( )
| A. | 除去乙酸乙酯中混有的乙酸,可以加入Na2CO3溶液,再分液 | |
| B. | 将SO2通入滴有酚酞的NaOH溶液中,溶液褪色,可以证明SO2具有漂白性 | |
| C. | 用金属钠分别与水和乙醇反应,可比较水分子中氢原子和乙醇羟基中氢原子的活泼性 | |
| D. | 先加盐酸酸化,再加入BaCl2溶液,生成白色沉淀,可确定该溶液中含有SO42- |
 SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如图所示的实验装置.检验该装置的气密性,先在试管中装入适量的水(保证玻璃导管的下端末在水中),然后(填操作方法)向外轻轻拉动注射器的活塞将会看到(填现象)浸没在水中的玻璃导管口有气泡冒出.则证明该装置气密性良好.
SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如图所示的实验装置.检验该装置的气密性,先在试管中装入适量的水(保证玻璃导管的下端末在水中),然后(填操作方法)向外轻轻拉动注射器的活塞将会看到(填现象)浸没在水中的玻璃导管口有气泡冒出.则证明该装置气密性良好.