题目内容
已知下列反应的热化学方程式:6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2H2(g)+O2(g)=2H2O(g)△H2C(s)+O2(g)=CO2(g)△H3则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为 (用△H1、△H2、△H3表示)
2H2(g)+O2(g)=2H2O(g)△H2C(s)+O2(g)=CO2(g)△H3则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为
考点:用盖斯定律进行有关反应热的计算
专题:
分析:根据盖斯定律,利用方程式的加减得出C3H5(ONO2)3分解成CO2、N2、H2O、O2的化学方程式,其反应热也要相应的加减,从而得出其热化学反应方程式.
解答:
解:已知:
①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②2H2(g)+O2(g)═2H2O(g)△H2
③C(s)+O2(g)═CO2(g)△H3
由盖斯定律:5×②+12×③-2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)
△H=12△H3+5△H2-2△H1;
故答案为:12△H3+5△H2-2△H1.
①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②2H2(g)+O2(g)═2H2O(g)△H2
③C(s)+O2(g)═CO2(g)△H3
由盖斯定律:5×②+12×③-2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)
△H=12△H3+5△H2-2△H1;
故答案为:12△H3+5△H2-2△H1.
点评:本题考查了反应热的计算,侧重于盖斯定律应用的考查,题目难度不大,准确把握盖斯定律的概念是关键.

练习册系列答案
相关题目
某元素基态原子的外围电子排布为3d54s2,则下列说法不正确的是( )
| A、该元素为Mn元素 |
| B、该元素原子核外有4个能层 |
| C、该元素原子最外层共有7个电子 |
| D、该元素属于d区元素 |
能正确表示下列反应的离子方程式是( )
| A、Na2O2加入水制备O2:2O22-+2H2O=4OH-+O2↑ |
| B、用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| D、向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
如图是某物质发生化学反应的示意图,其中“ ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子,则生成物甲的化学式为
”表示氢原子,则生成物甲的化学式为 ( )
( )
 ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子,则生成物甲的化学式为
”表示氢原子,则生成物甲的化学式为 ( )
( )| A、H2 |
| B、CO2 |
| C、H2O |
| D、CO |
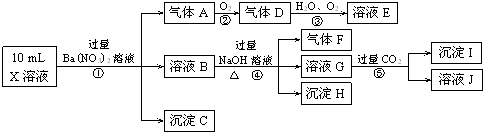
溶液X中可能含有K+、Mg2+、Al3+、AlO2-、SiO32-、CO32-、SO32-、SO42-中的若干种离子.某同学对该溶液进行了如下实验:

下列判断正确的是( )

下列判断正确的是( )
| A、气体甲一定是纯净物 |
| B、沉淀乙为Mg(OH)2 |
| C、沉淀甲是硅酸和硅酸镁的混合物 |
| D、溶液X中一定存在K+、AlO2-和SiO32-离子 |
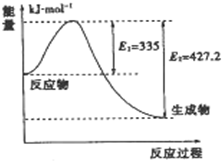 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.