题目内容
7.用下列装置能达到有关实验目的是( )
| A. | 甲图装置用标准液滴定待测液 | B. | 用乙图装置制备Fe(OH)2 | ||
| C. | 丙图装置可制得金属钾 | D. | 丁图验证NaHCO3和Na2CO3热稳定性 |
分析 A.氢氧化钠应该用碱式滴定管盛放,图示滴定管为酸式滴定管;
B.煤油的密度较小,可以起到隔绝空气的作用;
C.金属钾的活泼性大于铝,不能用铝热反应制取铝;
D.大试管中温度较高,应该将碳酸钠放入大试管中.
解答 解:A.图示滴定管为酸式滴定管,标准液为NaOH溶液,应该用碱式滴定管盛放,故A错误;
B.煤油浮在硫酸亚铁溶液上方,能够隔绝空气防止氢氧化亚铁氧化,可用乙图装置制备Fe(OH)2,故B正确;
C.铝热反应制取的金属活泼性小于Al,K的活泼性大于铝,无法通过铝热反应制备,故C错误;
D.验证NaHCO3和Na2CO3热稳定性时,应该将碳酸钠盛放中温度较高的大试管中,图示装置无法达到实验目的,故D错误;
故选B.
点评 本题考查化学实验方案的评价,题目难度不大,涉及氢氧化亚铁制备、中和滴定、碳酸钠和碳酸氢钠热稳定性实验、铝热反应等知识,明确常见化学实验基本操作方法即可解答,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
11.下列说法正确的是( )
| A. | 可以通过电解熔融AlCl3来冶炼铝 | |
| B. | HF的稳定性很强,是因为其分子间能形成氢键 | |
| C. | 非极性键不只存在于双原子单质分子中 | |
| D. | 分解反应都是吸热反应,化合反应都是放热反应 |
15.研究发现,含pm2.5的雾霾主要成分有SO2、NOx、CxHy及可吸入颗粒等.
(1)雾霾中能形成酸雨的物质是SO2、NOx
(2)NaClO2溶液可以吸收SO2、NO.在NaClO2溶液中通入含有SO2和NO的气体,反应温度为323K,NaClO2溶液浓度为5×10-3mol•L-1.反应一段时间后溶液中离子浓度的分析结果如表
①写出NaClO2溶液脱硝过程中主要反应的离子方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O
增加压强,NO的转化率提高(填“提高”“不变”或“降低”).
②由实验结果可知,脱硫反应速率大于脱硝反应速率(填“大于”或“小于”).
原因是:除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高

(3)图1电解装置可将SO2、NO转化为(NH4)2SO4,
①阴极的电极反应式是NO+5e-+6H+=NH4++H2O
②SO2、NO通入电解装置中的体积比为5:2
(4)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图2,脱硝率与温度,负载率(分子筛中催化剂的质量分数)的关系如图3
①写出该脱硝原理总反应的化学方程式6NO+3O2+2C2H4$\frac{\underline{\;催化剂\;}}{\;}$3N2+4CO2+4H2O
②为达到最佳脱硝效果,应采取的条件是350℃、负载率3%.
(1)雾霾中能形成酸雨的物质是SO2、NOx
(2)NaClO2溶液可以吸收SO2、NO.在NaClO2溶液中通入含有SO2和NO的气体,反应温度为323K,NaClO2溶液浓度为5×10-3mol•L-1.反应一段时间后溶液中离子浓度的分析结果如表
| 离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/(mol•L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
增加压强,NO的转化率提高(填“提高”“不变”或“降低”).
②由实验结果可知,脱硫反应速率大于脱硝反应速率(填“大于”或“小于”).
原因是:除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高

(3)图1电解装置可将SO2、NO转化为(NH4)2SO4,
①阴极的电极反应式是NO+5e-+6H+=NH4++H2O
②SO2、NO通入电解装置中的体积比为5:2
(4)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图2,脱硝率与温度,负载率(分子筛中催化剂的质量分数)的关系如图3
①写出该脱硝原理总反应的化学方程式6NO+3O2+2C2H4$\frac{\underline{\;催化剂\;}}{\;}$3N2+4CO2+4H2O
②为达到最佳脱硝效果,应采取的条件是350℃、负载率3%.
12.下列有关化学用语的表达正确的是( )
| A. | 甲醛的电子式: | B. | 乙醇分子的球棍模型: | ||
| C. |  的名称:3-甲基-2-丁烯 的名称:3-甲基-2-丁烯 | D. | CO2的分子模型示意图为: |
19.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将硫的酒精溶液滴入一定量的热水中得微蓝色透明液体,用激光笔照射 | 有丁达尔效应 | 微蓝色透明液体为胶体 |
| B | 将FeSO4高温强热,得红色固体,产生的气体通入BaCl2溶液 | 产生白色沉淀 | 白色沉淀为BaSO4和BaSO3 |
| C | 取将气体X分别通入品红溶液和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是乙烯 |
| D | 向溶液Y中滴加硝酸,再滴加BaCl2溶液 | 有白色沉淀 | Y中一定含有SO42- |
| A. | A、 | B. | B | C. | C | D. | D |
15.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 无论是风力发电还是火力发电,都是将化学能转化为电能 | |
| B. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| C. | 硫的氧化物和氮的氧化物是形成酸雨的主要物质 | |
| D. | “无磷洗涤剂”的推广使用,不能有效减少水体富营养化的发生 |
16. 已知CsCl晶体的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的相对分子质量可以表示为( )
已知CsCl晶体的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的相对分子质量可以表示为( )
 已知CsCl晶体的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的相对分子质量可以表示为( )
已知CsCl晶体的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为a cm,如图所示,则CsCl的相对分子质量可以表示为( )| A. | NA•a3•ρ | B. | $\frac{{{N_A}•{a^3}•ρ}}{6}$ | C. | $\frac{{{N_A}•{a^3}•ρ}}{4}$ | D. | $\frac{{{N_A}•{a^3}•ρ}}{8}$ |
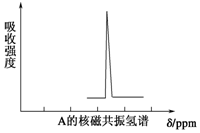 有一种新合成的高度对称的有机物A.已知10.4g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重7.2g和35.2g,经检验剩余气体为O2.
有一种新合成的高度对称的有机物A.已知10.4g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重7.2g和35.2g,经检验剩余气体为O2.
 ,其核磁共振氢谱有5个吸收峰.
,其核磁共振氢谱有5个吸收峰. 回答下列问题:
回答下列问题: