题目内容
含氮化合物是常见的化学物质,它们对人类的生产生活,有着重要的影响:

(1)氨气是合成其他含氮化合物的重要原料,也是实验室常用试剂.pH=9的氨水中由水电离的[OH-] mol?L-l,向浓度均为0.1mol?L-l的FeCl3、AlCl3溶液中缓慢通入足量的氨气,先生成的沉淀是 (填化学式),理由是 .注:Ksp[Fe(OH)3]=2.8×l0-39,Ksp[Al(OH)3]=1.3×l0-33
(2)氮氧化合物属于常见大气污染物,汽车尾气的排放是空气中氮氧化合物的主要来源,用尿素(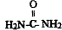 )做还原剂还原氮氧化合物是目前处理汽车尾气的一种方法,现设计实验模拟该过程并检验或收集其反应产物.
)做还原剂还原氮氧化合物是目前处理汽车尾气的一种方法,现设计实验模拟该过程并检验或收集其反应产物.
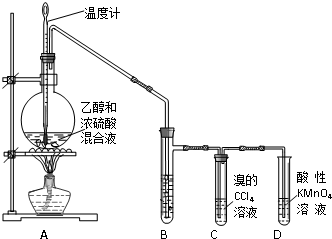
①用浓硝酸和铜片反应制取二氧化氮气体,发生装置应选择 (填所选如图1装置编号);
②将①所选装置与下面装置组装完毕后,应先 ,然后添加药品开始反应,将①所选装置中产生的二氧化氮气体通入下列装置进行相关实验.A装置可冷凝除去二氧化氮中的硝酸蒸气,其另一作用为 ;
③若实验过程中依次观察到下列现象:红棕色气体经过B装置变为无色;如图2C装置固体变为蓝色;图2D装置澄清石灰水变浑浊;E装置中收集到无色无味气体,遇空气不变色.试推测该反应的产物为 ,氧化剂、还原剂的物质的量之比为 ;
④图2C、D装置可否颠倒顺序 (填“可”或“否”),理由是 .

(1)氨气是合成其他含氮化合物的重要原料,也是实验室常用试剂.pH=9的氨水中由水电离的[OH-]
(2)氮氧化合物属于常见大气污染物,汽车尾气的排放是空气中氮氧化合物的主要来源,用尿素(
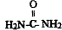 )做还原剂还原氮氧化合物是目前处理汽车尾气的一种方法,现设计实验模拟该过程并检验或收集其反应产物.
)做还原剂还原氮氧化合物是目前处理汽车尾气的一种方法,现设计实验模拟该过程并检验或收集其反应产物.①用浓硝酸和铜片反应制取二氧化氮气体,发生装置应选择
②将①所选装置与下面装置组装完毕后,应先
③若实验过程中依次观察到下列现象:红棕色气体经过B装置变为无色;如图2C装置固体变为蓝色;图2D装置澄清石灰水变浑浊;E装置中收集到无色无味气体,遇空气不变色.试推测该反应的产物为
④图2C、D装置可否颠倒顺序
考点:难溶电解质的溶解平衡及沉淀转化的本质,常见气体制备原理及装置选择
专题:
分析:(1)室温时,Kw=1×10-14,根据c(H+)×c(OH-)=1×10-14,以及H2O?H++OH-计算;根据Al(OH)3、Cu(OH)2的溶度积常数,物质的溶度积越小,越易形成沉淀;
(2)①用浓硝酸和铜片反应制取二氧化氮气体,属于固体与液体反应制取气体,反应不需要加热,据此分析发生装置;
②制取气体装置组装完毕,应先检查装置的气密性;A装置中装有氯化钙固体,氯化钙具有吸水性;
③二氧化氮通过尿素后,红棕色气体经过B装置变为无色;如图2C装置固体变为蓝色;图2D装置澄清石灰水变浑浊;E装置中收集到无色无味气体,遇空气不变色,说明生成气体有水蒸气、二氧化碳和氮气,尿素中N为-3价,C为+4价,二氧化氮中N为+4价,氧化剂为二氧化氮,还原剂为尿素,反应生成氮气,据得失电子守恒计算氧化剂与还原剂物质的量之比;
④先通过D装置,能够带出水蒸气,影响对水蒸气的检验.
(2)①用浓硝酸和铜片反应制取二氧化氮气体,属于固体与液体反应制取气体,反应不需要加热,据此分析发生装置;
②制取气体装置组装完毕,应先检查装置的气密性;A装置中装有氯化钙固体,氯化钙具有吸水性;
③二氧化氮通过尿素后,红棕色气体经过B装置变为无色;如图2C装置固体变为蓝色;图2D装置澄清石灰水变浑浊;E装置中收集到无色无味气体,遇空气不变色,说明生成气体有水蒸气、二氧化碳和氮气,尿素中N为-3价,C为+4价,二氧化氮中N为+4价,氧化剂为二氧化氮,还原剂为尿素,反应生成氮气,据得失电子守恒计算氧化剂与还原剂物质的量之比;
④先通过D装置,能够带出水蒸气,影响对水蒸气的检验.
解答:
解:(1)室温时,Kw=1×10-14,则
pH=9的氨水中c(OH-)=1×10-5mol/L,
则c(H+)=1×10-9mol/L,
又H2O?H++OH-,
则由水电离的c(OH-)=c(H+)=1×10-9mol/L,
根据Al(OH)3、Fe(OH)3的溶度积常数,在25℃下,向浓度均为0.1mol?L-1的AlCl3和FeCl3混合溶液中逐滴加入氨水,
<
,加入相同的浓度的氨水,Fe(OH)3最先析出,
故答案为:1×10-9;Fe(OH)3;Fe(OH)3的Ksp更小,所以先沉淀;
(2)①固体与液体反应制取气体,反应不需要加热,选择装置C,故答案为:C;
②制取气体装置组装完毕,应先检查装置的气密性;A装置中装有氯化钙固体,能够干燥气体,故答案为:检查装置的气密性;干燥气体;
③二氧化氮通过尿素后,红棕色气体经过B装置变为无色;如图2C装置固体变为蓝色;图2D装置澄清石灰水变浑浊;E装置中收集到无色无味气体,遇空气不变色,说明生成气体有水蒸气、二氧化碳和氮气,
尿素中N为-3价,二氧化氮中N为+4价,反应生成氮气中N为0价,其他元素价态不变,氧化剂为二氧化氮,1mol二氧化氮反应转移电子4mol,还原剂为尿素,1mol尿素反应转移电子物质的量为6mol,据得失电子守恒,氧化剂与还原剂物质的量之比为3:2,故答案为:水蒸气、二氧化碳和氮气;3:2;
④C检验水蒸气,D检验二氧化碳,若CD装置互换,无法证实水蒸气的存在,故答案为:否;无法证实水蒸气的存在.
pH=9的氨水中c(OH-)=1×10-5mol/L,
则c(H+)=1×10-9mol/L,
又H2O?H++OH-,
则由水电离的c(OH-)=c(H+)=1×10-9mol/L,
根据Al(OH)3、Fe(OH)3的溶度积常数,在25℃下,向浓度均为0.1mol?L-1的AlCl3和FeCl3混合溶液中逐滴加入氨水,
| 3 |
| ||
| 3 |
| ||
故答案为:1×10-9;Fe(OH)3;Fe(OH)3的Ksp更小,所以先沉淀;
(2)①固体与液体反应制取气体,反应不需要加热,选择装置C,故答案为:C;
②制取气体装置组装完毕,应先检查装置的气密性;A装置中装有氯化钙固体,能够干燥气体,故答案为:检查装置的气密性;干燥气体;
③二氧化氮通过尿素后,红棕色气体经过B装置变为无色;如图2C装置固体变为蓝色;图2D装置澄清石灰水变浑浊;E装置中收集到无色无味气体,遇空气不变色,说明生成气体有水蒸气、二氧化碳和氮气,
尿素中N为-3价,二氧化氮中N为+4价,反应生成氮气中N为0价,其他元素价态不变,氧化剂为二氧化氮,1mol二氧化氮反应转移电子4mol,还原剂为尿素,1mol尿素反应转移电子物质的量为6mol,据得失电子守恒,氧化剂与还原剂物质的量之比为3:2,故答案为:水蒸气、二氧化碳和氮气;3:2;
④C检验水蒸气,D检验二氧化碳,若CD装置互换,无法证实水蒸气的存在,故答案为:否;无法证实水蒸气的存在.
点评:本题考查了沉淀的溶度积和气体实验室制取和性质实验,题目难度较大.

练习册系列答案
相关题目
向1000mL某稀硝酸中加入5.6g铁粉,充分反应后,铁粉完全溶解并放出NO气体,溶液质量增加3.4g.则下列结论正确的是( )
| A、反应后的溶液中不含Fe2+ |
| B、放出的NO气体的体积在标准状况为2.24L |
| C、稀硝酸的物质的量浓度为0.2mol?L-1 |
| D、所得溶液中Fe2+和Fe3+的物质的量之比为4:1 |
下列有机化学方程式书写不正确的是( )
A、CH2CH=CH2+Br2→CH3- | |||
B、 +HNO3 +HNO3
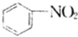 +H2O +H2O | |||
C、2CH3CH2OH+O2
| |||
D、CH3CH2OH+CH3COOH
|
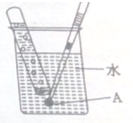
 如图为SO2的制备和收集装置图:(夹持仪器省略)
如图为SO2的制备和收集装置图:(夹持仪器省略)