题目内容
10.下列与实验相关的叙述正确的是( )| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| C. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
分析 A.稀释浓硫酸时,将浓硫酸倒入水中并不断搅拌;
B.配制溶液时,若加水超过容量瓶刻度,应该重新配制;
C.萃取剂不能和原溶剂互溶;
D.检验硫酸根离子时应该先加稀盐酸后加氯化钡溶液.
解答 解:A.稀释浓硫酸时,将浓硫酸倒入水中并不断搅拌,防止浓硫酸稀释过程中放出的热量导致溶液局部温度过高而溅出液体,故A错误;
B.配制溶液时,若加水超过容量瓶刻度,应该重新配制,因为吸出的溶液中还含有部分溶质,否则会导致配制溶液浓度偏低,故B错误;
C.萃取剂不能和原溶剂互溶,乙醇和水互溶,不能作碘水的萃取剂,应该用苯或四氯化碳,故C正确;
D.检验硫酸根离子时应该先加稀盐酸后加氯化钡溶液,排除碳酸根离子等离子的干扰,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及实验操作、萃取剂的选取、离子检验等知识点,明确实验原理及物质性质、实验操作方法是解本题关键,注意D中溶液滴加顺序,为易错点.

练习册系列答案
相关题目
18.下列离子方程式中,正确的是( )
| A. | 向水中加入金属钠:Na+H2O═Na++OH-+H2↑ | |
| B. | 用NaOH溶液检验NH4Cl溶液中的铵根离子:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- | |
| D. | 用食醋除去水瓶中的水垢:CO${\;}_{3}^{2-}$+2CH3COOH═2CH3COO-+CO2↑+H2O |
15.下列两种物质作用时,反应条件或反应物的用量比改变,生成的化合物不会改变的( )
| A. | 钠与氧气 | B. | 氢氧化钠与二氧化碳反应 | ||
| C. | 氧化钠与水反应 | D. | 木炭(C)和O2 |
19.如何用所提供的试剂和方法除去各粉末状混合物中的杂质(括号内为杂质).将所选答案的编号填入下表内相应的空格内(如果不需要外加试剂,则对应答案栏可空着).可供选择的试剂:A.盐酸 B.氢氧化钠溶液 C.氧气 D.水 E.二氧化碳
可选用的操作:①水洗 ②加热 ③高温灼烧 ④过滤 ⑤结晶
可选用的操作:①水洗 ②加热 ③高温灼烧 ④过滤 ⑤结晶
| 固体混合物 | 所选试剂 | 所选操作 | |
| (1) | CaCO3(SiO2) | ||
| (2) | NaCl(SiO2) | ||
| (3) | SiO2(Fe2O3) | ||
| (4) | SiO2(CaCO3) | ||
| (5) | SiO2(NH4Cl) |
6.对于可逆反应2SO2+O2?2SO3,在混合气中充入一定量的18O原子,达到平衡以后,18O原子( )
| A. | 只存在于O2中 | B. | 只存在于O2和SO2中 | ||
| C. | 只存在于O2和SO3中 | D. | 存在于O2、SO2和SO3中 |
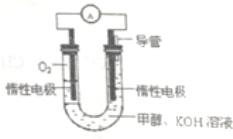 科学家预言,燃料电池将是21世纪获得电力的重要途径,美国己计划将甲醇燃料电池用于军事目的.一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在KOH电解液中直接加入纯化后的甲醇,同时向一个电极通入空气.
科学家预言,燃料电池将是21世纪获得电力的重要途径,美国己计划将甲醇燃料电池用于军事目的.一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在KOH电解液中直接加入纯化后的甲醇,同时向一个电极通入空气.