题目内容
下列化学用语的表述对应正确的是( )
| A、碳酸氢钠的电离方程式:NaHCO3═Na++H++CO32- | ||||
B、用铜做阳极电解氯化铜溶液的离子方程式:Cu2++2Cl-
| ||||
| C、小苏打水解的离子方程式:HCO3-+H2O?H3O++CO32- | ||||
| D、碳酸钙的溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq) |
分析:A.碳酸氢钠完全电离生成碳酸氢根离子和钠离子;
B.根据电解池工作原理可知,用铜做阳极铜溶解;
C.根据离子组成形式的变化来分析,HCO3-→CO32- 是电离反应;
D.沉淀溶解平衡时生成沉淀的速率和沉淀溶解的速率相同,是动态平衡.
B.根据电解池工作原理可知,用铜做阳极铜溶解;
C.根据离子组成形式的变化来分析,HCO3-→CO32- 是电离反应;
D.沉淀溶解平衡时生成沉淀的速率和沉淀溶解的速率相同,是动态平衡.
解答:解:A.碳酸氢钠完全电离生成碳酸氢根离子和钠离子,NaHCO3=Na++HCO3-,故A错误;
B.用铜做阳极电解氯化铜溶液,阳极Cu-2e-=Cu2+,阴极Cu2++2e-=Cu,故B错误;
C.H3O+即是H+,HCO3-+H2O?H3O++CO32-为小苏打的电离方程式,小苏打水解的离子方程式为:HCO3-+H2O?OH-+H2CO3,故C错误;
D.达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,是动态平衡,速率相等,方程式为:CaCO3(s)?Ca2+(aq)+CO32-(aq),故D正确;
故选D.
B.用铜做阳极电解氯化铜溶液,阳极Cu-2e-=Cu2+,阴极Cu2++2e-=Cu,故B错误;
C.H3O+即是H+,HCO3-+H2O?H3O++CO32-为小苏打的电离方程式,小苏打水解的离子方程式为:HCO3-+H2O?OH-+H2CO3,故C错误;
D.达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,是动态平衡,速率相等,方程式为:CaCO3(s)?Ca2+(aq)+CO32-(aq),故D正确;
故选D.
点评:本题主要考查了化学用语的表述,注意多元弱酸的酸根离子的水解和电离的区别,掌握电解的原理以及沉淀溶解平衡的含义是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
下列化学用语的表述对应正确的是
| A.碳酸氢钠的电离方程式:NaHCO3===Na++H++CO32- |
B.用铜做阳极电解氯化铜溶液的离子方程式:Cu2++2Cl-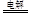 Cu+Cl2↑ Cu+Cl2↑ |
C.硫化钠水解的离子方程式:S2-+2H2O H2S+2OH- H2S+2OH- |
D.碳酸钙的溶解平衡:CaCO3(s)  Ca2+(aq) + CO32-(aq) Ca2+(aq) + CO32-(aq) |
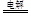 Cu+Cl2↑
Cu+Cl2↑ H2S+2OH-
H2S+2OH-