题目内容
已知A为蓝色溶液,B、C、I、K为单质,其余均为化合物,其中B、L、K 常温下为气体,且I为有色气体.G为黑色固体,F的焰色反应透过蓝色钴玻璃片显紫色.各物质转化关系如图:

回答下列问题:
(1)P的电子式是 ;
(2)C元素原子价电子排布式为: .

回答下列问题:
(1)P的电子式是
(2)C元素原子价电子排布式为:
考点:无机物的推断
专题:推断题
分析:A为蓝色溶液,含有Cu2+,电解A的溶液得到B、C、D三种物质,说明水与铜离子都发生放电,其中B、C为单质,且B为气体,则B为O2,C为Cu,D为酸,而Cu与D在常温下反应生成A、L、N,故D为HNO3,A为Cu(NO3)2,B与C生成E为CuO,G为黑色固体,作催化剂条件下J生成氧气与F,F的焰色反应透过蓝色钴玻璃片显紫色,则J为KClO3,F为KCl,G为MnO2,电解F与N得到H、I、K,则N为H2O,有色气体I为Cl2,气体单质H2,H为KOH,氯气与KOH反应生成P为KClO,则气体L为NO或二氧化氮,据此解答.
解答:
解:A为蓝色溶液,含有Cu2+,电解A的溶液得到B、C、D三种物质,说明水与铜离子都发生放电,其中B、C为单质,且B为气体,则B为O2,C为Cu,D为酸,而Cu与D在常温下反应生成A、L、N,故D为HNO3,A为Cu(NO3)2,B与C生成E为CuO,G为黑色固体,作催化剂条件下J生成氧气与F,F的焰色反应透过蓝色钴玻璃片显紫色,则J为KClO3,F为KCl,G为MnO2,电解F与N得到H、I、K,则N为H2O,有色气体I为Cl2,气体单质H2,H为KOH,氯气与KOH反应生成P为KClO,则气体L为NO或二氧化氮,
(1)P为KClO,电子式是 ,故答案为:
,故答案为: ;
;
(2)C为Cu,原子核外电子数为29,处于第四周期IB族,元素原子价电子排布式为:3d104s1,故答案为:3d104s1.
(1)P为KClO,电子式是
 ,故答案为:
,故答案为: ;
;(2)C为Cu,原子核外电子数为29,处于第四周期IB族,元素原子价电子排布式为:3d104s1,故答案为:3d104s1.
点评:本题考查无机物推断,注意根据电解产物、物质的颜色以及焰色反应进行推断,需要学生熟练掌握电解原理、元素化合物性质,难度中等.

练习册系列答案
相关题目
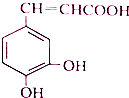
咖啡酸具有止血功效,存在于多种中药中,其结构简式如图,则下列有关说法正确的是( )

| A、该物质中苯环上一氯代物有2种 |
| B、1mol该物质可以与1.5mol碳酸钠溶液反应生成1.5mol的CO2 |
| C、既能发生取代反应,也能发生加成反应 |
| D、所有碳原子不可能都在同一平面上 |
某温度下,在一体积为2L的密闭容器中,通入112g N2 和24g H2,此时容器内压强为p大气压,在该温度和催化剂作用下,H2和N2 反应达到平衡,测得平衡时压强为0.95大气压,下列说法不正确的是( )
| A、平衡时,N2的物质的量是3.6mol |
| B、平衡时,H2的物质的量是10.8mol |
| C、平衡时,N2的转化率为10% |
| D、NH3的体积百分含量是10% |
β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1,下列说法不正确的是( )


| A、维生素A1难溶于水,也难溶于NaOH溶液 |
| B、β-紫罗兰酮与中间体X互为同系物 |
| C、1molβ-紫罗兰酮与1molCl2发生加成反应可得到3种不同产物 |
| D、β-紫罗兰酮能发生加成反应、取代反应、氧化反应、还原反应、加聚反应 |
化学与生活密切相关,下列有关说法正确的是( )
| A、地沟油,塑化剂(邻苯二甲酸酯类物质)均属于高分子化合物都对健康有害 |
| B、家用84消毒液可与清洁剂(主要是盐酸的溶液)混合使用,增强去污能力 |
| C、面粉厂、水泥厂常用静电除尘装置是根据胶体带电这一性质设计的 |
| D、酸雨形成主要来源于SO2或NOx排放所致 |
用惰性电极电解下列溶液,一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全恢复的是( )
| A、CuCl2(CuO) |
| B、NaOH(NaOH) |
| C、CuSO4[Cu (OH)2] |
| D、NaCl(HCl) |
在酸性无色溶液中,能大量共存的离子组是( )
| A、Mg2+、SO42-、HCO3-、Cl- |
| B、Na+、K+、Al3+、NO3- |
| C、Al3+、Cu2+、SO42-、Cl- |
| D、Na+、Ca2+、Cl-、CO32- |
 厨余垃圾经发酵后,通过电渗析法处理可富集乳酸,有关原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).
厨余垃圾经发酵后,通过电渗析法处理可富集乳酸,有关原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).