题目内容
已知在10l kPa下,1 g氢气在氧气中完全燃烧生成气态水时,放出热量120.9kJ.则下列说法中正确的是( )
| A、氢气的燃烧热为241.8 kJ?mol-1 | B、1 mol H2O(1)具有的能量大于1 mol H2O(g)具有的能量 | C、反应的热化学方程式为:2H2(g)+O2(g)=2H2O(g);△H=+483.6 kJ?mol-1 | D、2 mol H2(g)和1 mol O2(g)具有的能量总和大于2 mol H2O(g)具有的能量 |
分析:A、计算1molH2完全燃烧生成稳定氧化物液态水时放出的热量为氢气的燃烧热;
B、根据液态水具有的能量低于气态水具有的能量分析;
C、热化学方程式需要标注物质聚集状态,反应是放热反应,焓变为负值;
D、依据反应是放热反应和能量守恒分析判断.
B、根据液态水具有的能量低于气态水具有的能量分析;
C、热化学方程式需要标注物质聚集状态,反应是放热反应,焓变为负值;
D、依据反应是放热反应和能量守恒分析判断.
解答:解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,2g氢气燃烧生成液态水放出的热量为燃烧热,氢气的燃烧热数值大于241.8 kJ?mol-1,故A错误;
B、液态水具有的能量低于气态水具有的能量,所以1molH2O(l)具有的能量小于1molH2O(g)的能量,故B错误;
C、反应是放热反应,焓变为负值,4g氢气燃烧生成气态水放热483.6KJ,反应的热化学方程式:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ?mol-1,故C错误;
D、反应是放热反应,反应物能量高于生成物能量,即2molH2和1molO2的能量总和大于2molH2O(g)的能量,故D正确;
故选D.
B、液态水具有的能量低于气态水具有的能量,所以1molH2O(l)具有的能量小于1molH2O(g)的能量,故B错误;
C、反应是放热反应,焓变为负值,4g氢气燃烧生成气态水放热483.6KJ,反应的热化学方程式:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ?mol-1,故C错误;
D、反应是放热反应,反应物能量高于生成物能量,即2molH2和1molO2的能量总和大于2molH2O(g)的能量,故D正确;
故选D.
点评:本题考查了热化学方程式书写,燃烧热概念应用等知识,题目难度中等,注意反应前后能量守恒的分析判断,本题侧重对学生基础知识的训练和检验,有利于培养学生的分析、理解能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
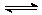 2SO3
(g) ;△H = -98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
2SO3
(g) ;△H = -98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量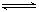 2SO3 (g) ;△H = -98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
2SO3 (g) ;△H = -98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量