题目内容
15.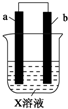 下列对如图所示装置实验现象的描述错误的是( )
下列对如图所示装置实验现象的描述错误的是( ) | a电极 | b电极 | X溶液 | |
| ① | Cu | Zn | CuCl2 |
| ② | Zn | 石墨 | HCl |
| A. | 实验①中a极质量增加 | B. | 实验①中Cl-离子向正极移动 | ||
| C. | 实验②a极质量减少 | D. | 实验②中b极放出无色气体 |
分析 实验①中Zn失电子作负极,Cu为正极,正极上铜离子得电子生成Cu;
实验②中中Zn失电子作负极,石墨为正极,正极上氢离子得电子生成氢气;
溶液中阴离子向负极移动,据此分析.
解答 解:A.实验①中a极上铜离子得电子生成Cu,a极质量增加,故A正确;
B.原电池中阴离子向负极移动,则Cl-离子向负极移动,故B错误;
C.实验②中中Zn失电子作负极,即a极质量减少,故C正确;
D.实验②中b极上氢离子得电子生成氢气,即b极放出无色气体,故D正确.
故选B.
点评 本题考查化学电源知识,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意原电池的两极上的变化以及原电池原理.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
5.25℃时,在10mL浓度均为0.1mol•L-1的盐酸和醋酸混合溶液中滴加0.1mol•L-1NaOH溶液,下列有关溶液中离子浓度关系正确的是( )
| A. | 未加NaOH溶液时,c(H+)>c(CI-)═c(CH3COOH) | |
| B. | 加入10mLNaOH溶液时:c(CH3COO-)+c(OH-)═c(H+) | |
| C. | 加入NaOH溶液至PH=7时:c(Na+)═c(CI-) | |
| D. | 加入20mLNaOH溶液时:c(Na+)═c(CH3COO-)+c(CI-) |
6.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | Na2O2中既含有离子键又含有非极性共价键 | |
| C. | KOH中只含有共价键 | |
| D. | KI和HI中化学键类型完全相同 |
3.可逆反应:2NO2$\stackrel{△}{?}$2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是:①单位时间内生成n molO2的同时生成2n molNO2②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态③混合气体的颜
色不再改变的状态④混合气体的密度不再改变的状态⑤混合气体的平均摩尔质量不再改变的状态 ⑥混合气体的压强不再改变的状态( )
色不再改变的状态④混合气体的密度不再改变的状态⑤混合气体的平均摩尔质量不再改变的状态 ⑥混合气体的压强不再改变的状态( )
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ①③⑤⑥ | D. | 全部 |
20.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 | |
| B. | 制作航天服的聚脂纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| C. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| D. | 重金属离子能杀死H7N9禽流感病毒 |
20.下列各组混合物能用分液漏斗直接分离的是( )
| A. | 植物油与汽油 | B. | 四氯化碳与水 | C. | 四氯化碳和碘 | D. | 水与乙醇 |
1.铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O═Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
| A. | 电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe | |
| B. | 电池放电时,负极反应为Fe-2e-═Fe2+ | |
| C. | 电池充电过程中,阴极附近溶液的pH升高 | |
| D. | 电池充电时,阳极反应为2Ni(OH)2+2OH--2e-═Ni2O3+3H2O |
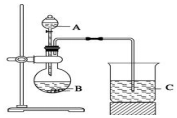 一组同学设计了如图装置来一次性完成验证C、Si、S非金属性强弱的实验
一组同学设计了如图装置来一次性完成验证C、Si、S非金属性强弱的实验