题目内容
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: | ||
B、CO2的电子式: | ||
C、中子数为20的氯原子:
| ||
| D、明矾的化学式:KAlSO4?12H2O |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.硫原子核电荷数为16,核外电子数为16;
B.二氧化碳分子中存在两个碳氧双键,不是碳氧单键;
C.氯元素的核电荷数为17,中子数为20的氯原子的质量数为37;
D.明矾为离子化合物,阴阳离子的正负电荷总数一定相等,明矾的化学式中总电荷数不等于0.
B.二氧化碳分子中存在两个碳氧双键,不是碳氧单键;
C.氯元素的核电荷数为17,中子数为20的氯原子的质量数为37;
D.明矾为离子化合物,阴阳离子的正负电荷总数一定相等,明矾的化学式中总电荷数不等于0.
解答:
解:A.硫原子核外电子数为16,其原子结构示意图为: ,故A错误;
,故A错误;
B.二氧化碳为共价化合物,分子中存在两个碳氧双键,二氧化碳的电子式为: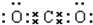 ,故B错误;
,故B错误;
C.中子数为20的氯原子的质量数为37,该原子可以表示为:
Cl,故C正确;
D.明矾的化学式:KAlSO4?12H2O,阴阳离子正电荷数不相等,明矾的化学式为:KAl(SO4)2?12H2O,故D错误;
故选C.
 ,故A错误;
,故A错误;B.二氧化碳为共价化合物,分子中存在两个碳氧双键,二氧化碳的电子式为:
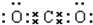 ,故B错误;
,故B错误;C.中子数为20的氯原子的质量数为37,该原子可以表示为:
37 17 |
D.明矾的化学式:KAlSO4?12H2O,阴阳离子正电荷数不相等,明矾的化学式为:KAl(SO4)2?12H2O,故D错误;
故选C.
点评:本题考查了电子式、化学式、原子结构示意图等知识,题目难度不大,注意掌握常见化学用语的表示方法,选项B为易错点,注意二氧化碳中的碳氧键为碳氧双键.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
 某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )| A、铜电极附近观察到黄绿色气体 |
| B、石墨电极附近溶液呈红色 |
| C、溶液中的Na+向石墨电极移动 |
| D、铜电极上发生还原反应 |
 图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu,b极:Fe-2e一=Fe2+,下列说法中不正确的是( )
图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu,b极:Fe-2e一=Fe2+,下列说法中不正确的是( )| A、该装置可能是电解池 |
| B、a极上发生的是还原反应 |
| C、a、b不可能是同种电极材料 |
| D、该装置工作时,溶液中的阴离子向b极移动 |
 如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置.则下列说法正确的是( )
如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置.则下列说法正确的是( )| A、甲装置中锌为负极,发生还原反应 |
| B、甲装置盐桥的作用是使反应过程中ZnSO4溶液和CuSO4溶液保持电中性 |
| C、乙装置中铁极为阳极,电极反应式为:2Na++2e-═2Na |
| D、乙装置中B是氯气出口,A是钠出口 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、1mol乙烷分子所含质子数为30NA |
| B、28gC2H4所含共用电子对数目为6NA |
| C、1L0.1mol?L-1乙酸溶液中H+数为0.1NA |
| D、标准状况下,22.4L乙醇的分子数为NA |