题目内容
管道煤气的主要成分是H2、CO和少量的甲烷。相应的热化学方程式为:2H2(g)+O2(g)![]() 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-566 kJ·mol-1
2CO2(g) ΔH=-566 kJ·mol-1
CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的燃气,理论上所获得的热值,后者大约是前者的多少倍( )
解析:相同条件下等体积的气体的物质的量相同,设CH4为2 mol,H2、CO共2 mol,各1 mol(生成水煤气的反应为:C+H2O![]() CO+H2)。题目所求为:
CO+H2)。题目所求为: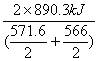 ≈3.1。
≈3.1。
答案:D

(1)目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
2CO+O2![]() 2CO2 2H2+O2
2CO2 2H2+O2![]() 2H2O CH4+2O2
2H2O CH4+2O2![]() CO2+2H2O
CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是____________。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是______________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是________________________。
(2)管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 |
熔点/℃ | -183.3 | -189.7 | -138.4 |
沸点/℃ | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是_____________________________________________________________________。
目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
2CO+O2![]() 2CO2 2H2+O2
2CO2 2H2+O2![]() 2H2O CH4+2O2
2H2O CH4+2O2![]() CO2+2H2O
CO2+2H2O
根据以上化学方程式判断:
(1)燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是________。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是________________。
(2)管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 |
熔点(℃) | -183.3 | -189.7 | -138.4 |
沸点(℃) | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是____________________________________________________________。