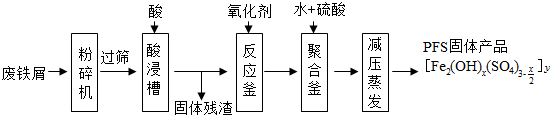
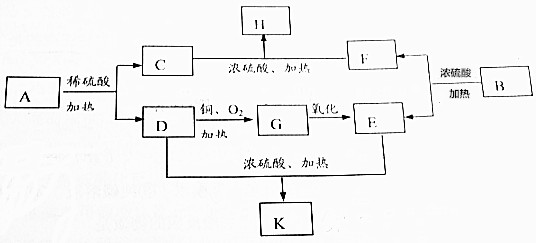
��Ŀ����
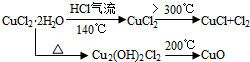
9��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ�CuCl2•2H2O�Ʊ�CuCl�����������̽���������ϲ��ġ�
��ʵ��̽����
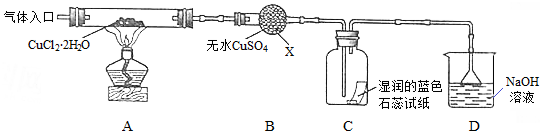
��С������ͼ��ʾװ�ý���ʵ�飨�г������ԣ���
��ش��������⣺
��1������X�����������θ���ܣ�
��2��ʵ��������Ⱥ�˳����a��c-d-b��e��������ı�ţ�
a�����װ�õ������Ժ����ҩƷ
b��Ϩ��ƾ��ƣ���ȴ
c���ڡ�������ڡ���ͨ�����HCl
d����ȼ�ƾ��ƣ�����
e��ֹͣͨ��HCl��Ȼ��ͨ��N2
��3����ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯������Ϊ��ɫ������ɫ��
��4��װ��D�з�����������ԭ��Ӧ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O��
��̽����˼��
��5����Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����������Ϣ������
����������CuCl2���������ԭ���Ǽ���ʱ�䲻����¶�ƫ�ͣ�
����������CuO���������ԭ����ͨ��HCl�������㣮
���� �ȷֽ�CuCl2•2H2O�Ʊ�CuCl��Ϊ����ˮ�⣬�������ͨ��HCl���壬Ȼ�����A���Թܣ�XΪ���θ���ܣ�X����ˮ����ͭ��������֪CuCl2•2H2O�ֽ�����ˮ����C����ֽ�ȱ�����ɫ����֪����2CuCl2$\frac{\underline{\;����300��\;}}{\;}$2CuCl+Cl2����D��NaOH��Һ����β����ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����CuCl2���¶Ȳ��������ʱ�䲻���йأ�����CuO��û����HCl�ķ�Χ�м��Ȼ���δ���Թ���ȴ��ֹͣͨ��HCl�����йأ��Դ������
��� �⣺��1����ͼ��������������֪������X������Ϊ���θ���ܣ��ʴ�Ϊ�����θ���ܣ�
��2��ʵ�������������ɣ��ȼ���װ�õ������ԣ����ȷֽ�CuCl2•2H2O�Ʊ�CuCl����ֹCuCl��������Cu+ˮ�����Ա���Ҫ�ȸ���װ���е�������ˮ������ż��ȣ���Ҫ��HCl�����м����Ʊ�����Ӧ��������Ϩ��ƾ��ƣ�Ӧ��Ҫ����ͨ�뵪��ֱ��װ����ȴ�����Բ���˳��Ϊ��a-c-d-b-e��
�ʴ�Ϊ��c-d-b��
��3��B���а�ɫ��Ϊ��ɫ��˵����ˮ���ɣ������л���Cl2������C��ʯ����ֽ����Ϊ��ɫ������ɫ��
�ʴ�Ϊ��ʯ����ֽ����Ϊ��ɫ������ɫ��
��4��D����Cl2��NaOH��Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��5������2CuCl2$\frac{\underline{\;����300��\;}}{\;}$2CuCl+Cl2����������CuCl2˵��CuCl2û�з�Ӧ��ȫ���ֽ��¶Ȳ��ߣ��ʴ�Ϊ������ʱ�䲻����¶�ƫ�ͣ�
������������ͭ��˵��CuCl�����������Ų�����CuO��˵��װ������������������û����HCl�ķ�Χ�м��Ȼ���δ���Թ���ȴ��ֹͣͨ��HCl���壬�ʴ�Ϊ��ͨ��HCl�������㣮
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��ԭ����ʵ��װ�õ����á�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��Ԫ�ػ�������ʵ�����ϵ�ѵ������5��Ϊ�����ѵ㣬��Ŀ�Ѷ��еȣ�

 ���ƿ�����ϵ�д�
���ƿ�����ϵ�д� ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�| A�� | HCl������ˮ | B�� | I2������ˮ | C�� | Cl2������ˮ | D�� | CO2������ˮ |
| A�� | ����ܽ���ϡ��������ȡ���� | B�� | �����Ϸ��ֿ�ű��ҩ������ | ||
| C�� | �ɶ����з������ѽ���� | D�� | ��°������Ƽ |
��1��NaClO2�Ļ�ѧ����Ϊ�������ƣ�
��2���ڹ��ݷ�Ӧ����ͨ�뺬SO2��NOx����������Ӧ�¶�323K��NaClO2��ҺŨ��Ϊ5��10-3mol•L-1����Ӧһ��ʱ�����Һ������Ũ�ȵķ�����������
| ���� | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/��mol•L-1�� | 8.35��10-4 | 6.87��10-6 | 1.5��10-4 | 1.2��10-5 | 3.4��10-3 |
���������շ�Ӧ�Ľ��У����ռ���Һ��pH��С������������䡱��С������
����ʵ������֪������Ӧ���ʴ���������Ӧ���ʣ�����ڡ���С�ڡ���ԭ���dz���SO2��NO�������г�ʼŨ�Ȳ�ͬ����������NO�ܽ�Ƚϵͻ�������Ӧ��ܽϸߣ�
��3���ڲ�ͬ�¶��£�NaClO2��Һ���������ķ�Ӧ��SO2��NO��ƽ���ѹPe��ͼ��ʾ��
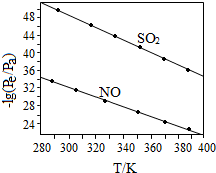
����ͼ������֪����Ӧ�¶����ߣ�����������Ӧ��ƽ�ⳣ������С������������䡱��С������
�ڷ�ӦClO2-+2SO32-�T2SO42-+Cl-��ƽ�ⳣ��K����ʽΪ$\frac{c��C{l}^{-}��{c}^{2}��S{{O}_{4}}^{2-}��}{c��Cl{{O}_{2}}^{-}��{c}^{2}��S{{O}_{3}}^{2-}��}$��
��4���������NaClO��Ca��ClO��2���NaClO2��Ҳ�ܵõ��Ϻõ���������Ч����
�ٴӻ�ѧƽ��ԭ��������Ca��ClO��2���NaClO���е��ŵ����γ�CaSO4��������Ӧƽ������﷽���ƶ���SO2ת������ߣ�
����֪���з�Ӧ��
SO2��g��+2OH-��aq���TSO32-��aq��+H2O��l����H1
ClO-��aq��+SO32-��aq���TSO42-��aq��+Cl-��aq����H2
CaSO4��s���TCa2+��aq��+SO42-��aq����H3
��ӦSO2��g��+Ca2+��aq��+ClO-��aq��+2OH-��aq���TCaSO4��s��+H2O��l��+Cl-��aq���ġ�H=��H1+��H2-��H3��
| A�� | KOH | B�� | KNO3 | C�� | NH4HCO3 | D�� | �ƾ� |
| ʵ��һ | ʵ��� | |
| װ�� | 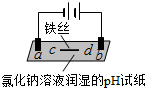 | 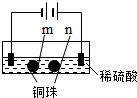 |
| ���� | a��d����ֽ������b����죬�ֲ���ɫ��c�������Ա仯 | ����ʯī�缫���������ݲ�����n�������ݲ������� |
| A�� | a��d����2H2O+2e-�TH2��+2OH- | |
| B�� | b����2Cl--2e-�TCl2�� | |
| C�� | c�������˷�Ӧ��Fe-2e-�TFe2+ | |
| D�� | ����ʵ��һ��ԭ����ʵ�����m��������ͭ |
| A�� | SiO2$\stackrel{HCl��aq��}{��}$SiCl4$��_{����}^{H_{2}}$Si | |
| B�� | FeS2$��_{����}^{O_{2}}$SO2$\stackrel{H_{2}O}{��}$H2SO4 | |
| C�� | N2$��_{���¡���ѹ������}^{H_{2}}$NH3$\stackrel{HCl��aq��}{��}$NH4Cl��aq�� | |
| D�� | MgCO3$\stackrel{HCl��aq��}{��}$MgCl2��aq��$\stackrel{���}{��}$Mg |