题目内容
在温度为150 ℃条件下,向密闭容器中充入1 mol丙烯(C3H6)和甲烷的混合气体,再充入足量的氧气,完全燃烧后再恢复到150 ℃。欲使丙烯和甲烷混合气体对氢气的相对密度≥15.8,且反应后气体分子增加的总物质的量≤0.4 mol。问丙烯和甲烷的物质的量之比应满足什么关系?
解析:这是一个同时要满足两个条件的范围计算题。首先分析第一个条件,要求![]() ≥15.8,实际上是要求混合气体的平均相对分子质量≥15.8×2。
≥15.8,实际上是要求混合气体的平均相对分子质量≥15.8×2。
若设丙烯的物质的量为x mol,则甲烷的物质的量为(1-x) mol。
依题意有42x+16(1-x)≥15.8×2
解之得x≥0.6,所以![]()
再分析第二个条件,先写出化学方程式。
CH4+2O2![]() CO2+2H2O ①
CO2+2H2O ①
2C3H6+9O2![]() 6CO2+6H2O ②
6CO2+6H2O ②
因甲烷在燃烧前后体积不变,故反应后增加的物质的量只需通过②式便能建立满足条件的关系式,设丙烯的物质的量为y
2C3H6+9O2![]() 6CO2+6H2O Δn
6CO2+6H2O Δn
2 mol 1 mol
y mol 0.4 mol
又因为总物质的量增加随C3H6的含量减少而减少,所以有![]() ≤
≤![]() ,y≤0.8,
,y≤0.8,![]()
因此![]() 时,可以同时满足两个条件。
时,可以同时满足两个条件。
故答案为![]() 。
。
答案:![]()

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目

 CO(g)+3H2(g);△H=+QkJ/mol(Q>0)
CO(g)+3H2(g);△H=+QkJ/mol(Q>0)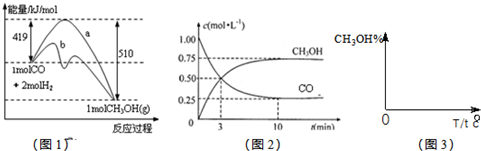



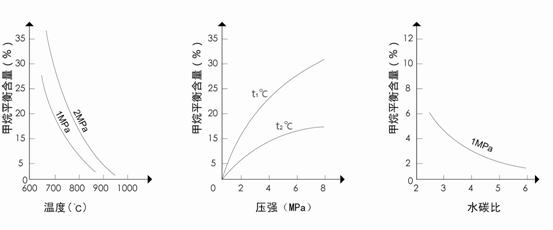
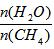 ]对甲烷蒸汽转化反应的影响如下图:
]对甲烷蒸汽转化反应的影响如下图: