题目内容
18.一定温度下,在一个容积为1L的密闭容器中,充入1mol H2(g)和1mol I2(g),发生反应H2(g)+I2(g)?2HI(g),经充分反应达到平衡后,HI(g)的气体体积分数为50%,在该温度下,在另一个容积为2L的密闭容器中充入1mol HI(g)发生反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g),则下列判断正确的是( )| A. | 第二个反应的平衡常数为1 | |
| B. | 第二个反应的平衡常数为0.05 | |
| C. | 第二个反应达到平衡时,H2的平衡浓度为0.25mol/L | |
| D. | 第二个反应达到平衡时,HI(g)的平衡浓度为0.25 mol/L |
分析 一定温度下,将H2和I2各1mol的气态混合物充入1L的密闭容器中,充分反应,达到平衡后生成的HI(g)的气体体积的50%,设转化的氢气为xmol,依据化学平衡三段式列式为:
H2 +I2 ?2HI
起始量(mol/L) 1 1 0
变化量(mol/L) x x 2x
平衡量(mol/L) 1-x 1-x 2x
HI(g)的气体体积的50%,则$\frac{2x}{1-x+1-x+2x}$=50%,解得x=0.5mol
故K=$\frac{1{\;}^{2}}{0.5×0.5}$=4,
该温度下,在另一个容积为2L的密闭容器中充入1mol HI(g)发生反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g),等效为充入H2和I2各0.5mol,又该反应为气体体积不变得反应故与原平衡成比例等效,则新平衡时氢气为0.5mol×$\frac{1}{2}$=0.25mol,HI(g)为1mol×$\frac{1}{2}$=0.5mol,以此解答该题.
解答 解:A、B.根据平衡常数只与温度有关,结合正反应与逆反应的平衡常数成倒数关系,故 2HI?H2 +I2的平衡常数为$\frac{1}{4}$,又同一反应平衡常数与系数成幂次方关系,故后一反应的平衡常数为$\sqrt{\frac{1}{4}}$=0.5,故A、B错误;
C.根据以上计算第二个反应达到平衡时,H2的平衡浓度为$\frac{0.25mol}{2L}$=0.125mol/L,故C错误;
D.由以上计算后第二反应达到平衡时,HI(g)的平衡浓度为$\frac{0.5mol}{2L}$=0.25mol/L,故D正确.
故选D.
点评 本题考查了化学平衡的三段式计算应用,为高考常见题型,侧重于学生的分析能力和计算能力的考查,平衡常数与方程式之间的关系以及等效平衡的判断是本题的关键,题目较简单.

 名师金手指领衔课时系列答案
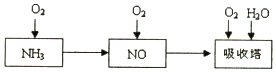
名师金手指领衔课时系列答案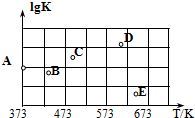 氯化亚砜用于医药、农药、染料工业及有机合成工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.工业上用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g).
氯化亚砜用于医药、农药、染料工业及有机合成工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.工业上用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g).(1)在373K时,向2L的密闭容器中通入SO2、SCl2与Cl2均为0.04mol,发生上述反应.测得其压强(p)随时间(t)的变化为表中数据I(反应达到平衡时的温度与起始温度相同).
| t/min | 0 | 1 | 2 | 3 | 4 | 5 | |
| I | p | 6.0p0 | 6.7p0 | 6.1p0 | 5.4p0 | 5.0p0 | 5.0p0 |
| II | p | 6.0p0 | 7.0p0 | 5.3p0 | 5.0p0 | 5.0p0 | 5.0p0 |
①该反应的△H<(填“>”“<”或“=”)0.
②反应开始至达到平衡时,v(SOCl2)=0.005mol/(L•min).
③若只改变某一条件,其他条件相同时,测得其压强随时间的变化为表中数据II,则改变的条件是使用催化剂.
(2)如图是某同学测定上述反应的平衡常数的对数值(lgK)与温度的变化关系点.
①A点的数值为2.6.(已知:lg4=0.6)
②当升高到某一温度时,反应重新达到平衡,A点可能变化为BE点.
(3)已知反应S4(g)+4Cl2(g)═4SCl2(g) 的△H=-4kJ•mol-1,1molS4(g)、1molSCl2(g)分子中化学键断裂时分别需要吸收1064kJ、510kJ的能量,则1molCl2(g)分子中化学键断裂时需吸收的能量为243kJ.
(4)某种锂电池的负极由金属锂构成,正极由二氯亚砜(SOCl2)和碳材料构成.总反应为:4Li+2SOCl2═4LiCl+S+SO2↑,此种锂电池是一次电池,在放电时有气体产生.此电池工作时正极的电极反应式为2SOCl2+4e-=S+SO2↑+4Cl-,电解质中锂离子定向移向正极极(填“正极”或“负极”).
| A. | 夏天打开啤酒盖,喷出大量泡沫 | |
| B. | 工业上合成氨气时采用高温利于氨气的合成 | |
| C. | 在HI的分解实验达到平衡后加压颜色变深 | |
| D. | 锌和稀硫酸制备氢气时滴入少量硫酸铜可以加快速率 |
| A. | 足量铁在1molCl2中燃烧时转移电子数为2NA | |
| B. | 2L0.1mol•L-1氯化钾溶液中阴离子所带电荷数为NA | |
| C. | 1L0.1mol•L-1的Na2CO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| D. | 标准状况下,体积各为2.24L的HCl和NH3混合气体中含有的共价键数为0.25NA |
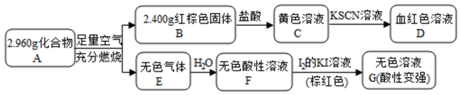
 . 该反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑.
. 该反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑.