题目内容
下列叙述正确的是( )
A、乙酸的键线式是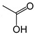 |
B、间二甲苯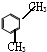 又叫2,4-二甲苯 又叫2,4-二甲苯 |
C、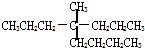 的最长碳链有7个C原子 的最长碳链有7个C原子 |
D、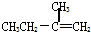 的名字读作:3位甲基3丁烯 的名字读作:3位甲基3丁烯 |
考点:有机化合物命名
专题:
分析:A.乙酸中含-COOH,键线表示单键;
B.取代基的位次和最小;
C.最长碳链有8个C原子;
D.从离官能团近的一端命名.
B.取代基的位次和最小;
C.最长碳链有8个C原子;
D.从离官能团近的一端命名.
解答:
解:A.乙酸中含-COOH,键线表示单键,则键线式为 ,故A正确;
,故A正确;
B.取代基的位次和最小,应为1,3二甲苯,故B错误;
C. 的最长碳链有8个C原子,故C错误;
的最长碳链有8个C原子,故C错误;
D.从离官能团近的一端命名,应为:2-甲基-1-丁烯,故D错误.
故选A.
 ,故A正确;
,故A正确; B.取代基的位次和最小,应为1,3二甲苯,故B错误;
C.
 的最长碳链有8个C原子,故C错误;
的最长碳链有8个C原子,故C错误;D.从离官能团近的一端命名,应为:2-甲基-1-丁烯,故D错误.
故选A.
点评:本题考查了有机物的命名,需要熟练掌握常见有机物的命名原则,如含有双键、三键,应该从距离三键、双键最近一端编号,本题难度中等.

练习册系列答案
相关题目
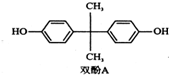 由于双酚A对婴儿发育、免疫力有影响,欧盟从2011年3月1日起禁止生产双酚A塑料奶瓶.双酚A简称双酚基丙烷,结构如图.下列分析不正确的是( )
由于双酚A对婴儿发育、免疫力有影响,欧盟从2011年3月1日起禁止生产双酚A塑料奶瓶.双酚A简称双酚基丙烷,结构如图.下列分析不正确的是( )| A、其分子式为C15H16O2 |
| B、它有弱酸性,且能和酸性高锰酸钾溶液反应 |
| C、它常温下呈液态,不溶于水,是苯酚的同系物 |
| D、双酚A分子中碳原子不可能在同一平面上 |
下列各溶液中,微粒的物质的量浓度关系不正确的是( )
| A、1.0mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| B、1.0mol/L NH4Cl溶液:c(NH4+)=c(Cl-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应,(假设容器不参加反应).若过滤后滤渣能被磁铁吸引,则下列有关叙述正确的是( )
| A、溶液中肯定不存在的离子只有Fe3+ |
| B、Fe3+和Cu2+均能被铁粉还原 |
| C、Fe2+与SCN-能形成红色的物质 |
| D、滤渣中肯定不含有铜 |
某溶液中除了H+、OH-以外,还含有大量的Mg2+、Fe3+、Cl-,且这三种离子的物质的量浓度之比为1:1:6,下列有关该溶液判断正确的是( )
| A、向该溶液中加入KI溶液后,原有的5种离子的物质的量不变 |
| B、向该溶液中滴加稀NaOH溶液,立即出现白色沉淀 |
| C、向该溶液中加入过量铁粉,只发生置换反应 |
| D、若溶液中c (Cl-)=0.6mol/L,则该溶液的pH=1 |
下列叙述正确的是( )
| A、常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
| B、Na的金属活性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C、HClO见光会分解,故氯水保存在棕色试剂瓶中 |
| D、Fe在Cl2中燃烧生成FeCl3,故在与其它非金属反应的产物中的Fe也显+3价 |
在密闭容器中一定量混合气体发生反应:xA (g)+yB(g)?zC(g),平衡时测得A的浓度为0.5mol?L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为0.2mol?L-1,下列判断正确的是( )
| A、平衡向正反应方向移动 |
| B、x+y>z |
| C、C的体积分数保持不变 |
| D、B的转化率降低 |
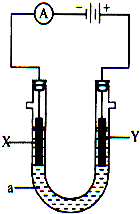 电解原理在化学工业中有广泛应用.如图示,是一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图示,是一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: