题目内容
13.将HCl、H2SO4、Ba(NO3)2三种溶液,按一定顺序滴入到Na2CO3溶液中至恰好完全反应有以下现象:①加入A时生成白色沉淀;
②往①沉淀中加入B时沉淀溶解,并有气体逸出;
③往②生成的溶液中加入C时,又有白色沉淀生成.
根据上述现象,回答:
(1)A、B、C各是什么溶液?(填溶质的化学式)
A.Ba(NO3)2 B.HCl C.H2SO4
(2)写出上述①②反应的离子方程式.Ba2++CO32-=BaCO3↓、BaCO3+2H+=Ba2++CO2↑+H2O.
分析 ①能和碳酸钠反应生成白色沉淀的是硝酸钡;
②再滴加B时沉淀溶解,并有气体逸出,则B为盐酸;因硫酸能和钡离子反应生成硫酸钡白色沉淀,
③往生成的溶液中加入C时,又有白色沉淀生成,则C为硫酸,以此分析判断A、B、C各物质,结合化学用语来解答.
解答 解:①能和碳酸钠反应生成白色沉淀的是硝酸钡;②再滴加B时沉淀溶解,并有气体逸出,则B为盐酸;因硫酸能和钡离子反应生成硫酸钡白色沉淀,③往生成的溶液中加入C时,又有白色沉淀生成,则C为硫酸,
(1)通过以上分析知,A是 Ba(NO3)2 B是HCl,C是硫酸.故答案为:Ba(NO3)2;HCl;H2SO4;
(2)①钡离子和碳酸根离子反应生成碳酸钡白色沉淀,离子方程式为Ba2++CO32-=BaCO3↓,②碳酸钡和盐酸反应生成钡离子、二氧化碳和水,离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,
故答案为:Ba2++CO32-=BaCO3↓、BaCO3+2H+=Ba2++CO2↑+H2O.
点评 本题以元素化合物的推断为载体考查了元素化合物的性质,明确各物质的性质是解本题的关键,注意在解题时问题的要求,把握化学用语的使用,题目难度中等.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
3.取一定质量镁铝合金,溶于足量盐酸,加过量NaOH溶液,滤出沉淀,加强热灼烧,得白色粉末,干燥后称量,这些粉末与原合金质量相等,则原合金中铝的质量分数为( )
| A. | 30% | B. | 40% | C. | 60% | D. | 70% |
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 室温下,1L pH=13的氢氧化钡溶液所含OH- 数为0.2NA | |
| B. | 标准状况下,0.1molAl3+含有的核外电子数为0.3 NA | |
| C. | 常温下,44gCO2中含有2NA个碳氧双键 | |
| D. | 将1 molN2 和3mol H2 通入密闭容器中,一定条件下充分反应,转移电子数为6NA |
1.实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示:

请回答下列问题:
(1)写出制备1,2二溴乙烷的反应原理方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2═CH2+Br2→BrCH2CH2Br.
(2)在此制备实验中,要尽可能迅速地把反应温度升高到170℃左右,最主要的目的是d(填序号).
a.引发反应 b.加快反应速度c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是判断装置是否堵塞.
(4)在装置C中应加入c(填序号),其目的是吸收反应中可能生成的酸性气体.
a.水b.浓硫酸c.氢氧化钠溶液d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是D中溴水的颜色完全褪去.
(6)将1,2二溴乙烷粗产品置于分液漏斗中,加水振荡后静置,产物应在下(填“上”或“下”)层.
(7)若产物中有少量副产物乙醚,可用蒸馏的方法除去.

| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)写出制备1,2二溴乙烷的反应原理方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O、CH2═CH2+Br2→BrCH2CH2Br.
(2)在此制备实验中,要尽可能迅速地把反应温度升高到170℃左右,最主要的目的是d(填序号).
a.引发反应 b.加快反应速度c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是判断装置是否堵塞.
(4)在装置C中应加入c(填序号),其目的是吸收反应中可能生成的酸性气体.
a.水b.浓硫酸c.氢氧化钠溶液d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是D中溴水的颜色完全褪去.
(6)将1,2二溴乙烷粗产品置于分液漏斗中,加水振荡后静置,产物应在下(填“上”或“下”)层.
(7)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
20.下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2和盐酸; Cu(OH)2和CH3COOH | |
| B. | BaCl2和Na2SO4; Ba(OH)2和CuSO4 | |
| C. | NaHCO3和NaHSO4 Na2CO3和NaHSO4 | |
| D. | NaHCO3( 过量)和Ca(OH)2 Ca(HCO3)2 和NaOH( 过量) |
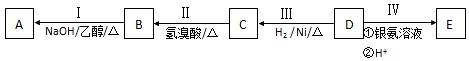
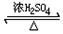 (CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O;
(CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O; 和
和 ;
; .
.

 ≈4.0]。
≈4.0]。