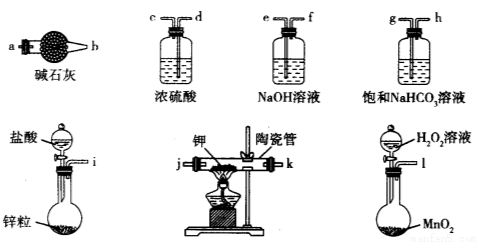
题目内容
按要求填空,(每空2分,共6分)
双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:_______________
(2)写出实验室用双氧水制取氧气的化学方程式:
(3)鉴于H2O2显弱酸性,它可以同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:______________
(1)H2O2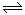 H++HO2-、HO2-
H++HO2-、HO2-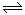 H++ O22-
H++ O22-
(2)2H2O2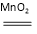 2H2O+O2↑
2H2O+O2↑
(3)H2O2 + Ba(OH)2 == BaO2 +2H2O
【解析】
试题分析:(1)把H2O2看成是二元弱酸,则在水溶液中部分电离产生氢离子,电离方程式是H2O2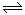 H++HO2-、HO2-
H++HO2-、HO2-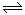 H++ O22-
H++ O22-
(2)过氧化氢在二氧化锰作催化剂的条件下分解生成水和氧气,化学方程式为2H2O2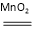 2H2O+O2↑;
2H2O+O2↑;
(3)H2O2看成是二元弱酸,与氢氧化钡反应生成的正盐是BaO2 ,所以过氧化氢与氢氧化钡反应生成过氧化钡和水,化学方程式为H2O2 + Ba(OH)2 == BaO2 +2H2O。
考点:考查对过氧化氢的认识,酸碱中和反应化学方程式的书写

练习册系列答案
相关题目