题目内容
下列对0.2mo1/LNa2SO4溶液叙述不正确的是(NA表示阿伏加德罗常数的值)( )
| A、1L溶液中含0.4NA个Na+ |
| B、1L溶液中含Na+和SO42-总数为0.8NA |
| C、2L溶液中含有0.4NA个SO42- |
| D、2L溶液中Na+的物质的量浓度为0.4mol/L |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.根据n=cv以及硫酸钠的组成来计算;
B.根据n=cv以及硫酸钠的组成来计算;
C.根据n=cv以及硫酸钠的组成来计算;
D.根据溶液的浓度与体积无关,离子浓度=溶质浓度×离子数.
B.根据n=cv以及硫酸钠的组成来计算;
C.根据n=cv以及硫酸钠的组成来计算;
D.根据溶液的浓度与体积无关,离子浓度=溶质浓度×离子数.
解答:
解:A.该溶液中Na2SO4的物质的量n=cv=1L×0.2mol/L=0.2mol,含有的Na+的物质的量等于Na2SO4的物质的量的2倍,为0.4mol,含0.4NA个Na+,故A正确;
B.该溶液中Na2SO4的物质的量n=cv=1L×0.2mol/L=0.2mol,含有的Na+的物质的量0.4mol,SO42-物质的量0.2mol,1L溶液中含Na+和SO42-总数为0.6NA,故B错误;
C.2L溶液中Na2SO4的物质的量n=cv=2L×0.2mol/L=0.4mol,含有0.4NA个SO42-,故C正确;
D.2L溶液中Na+的物质的量浓度=0.2mol/L×2L=0.4mol/L,故D正确;
故选:B.
B.该溶液中Na2SO4的物质的量n=cv=1L×0.2mol/L=0.2mol,含有的Na+的物质的量0.4mol,SO42-物质的量0.2mol,1L溶液中含Na+和SO42-总数为0.6NA,故B错误;
C.2L溶液中Na2SO4的物质的量n=cv=2L×0.2mol/L=0.4mol,含有0.4NA个SO42-,故C正确;
D.2L溶液中Na+的物质的量浓度=0.2mol/L×2L=0.4mol/L,故D正确;
故选:B.
点评:本题主要考查了物质的量的概念与计算,难度不大,根据所学知识即可完成.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
下列说法正确的是( )
| A、在氧化还原反应中,氧化剂经化学变化变成还原剂 |
| B、在氧化还原反应中,氧化剂被氧化,还原剂被还原 |
| C、在化学反应中,能把其他物质氧化的物质是氧化剂 |
| D、在氧化还原反应中,还原剂生成的氧化产物一定只具有氧化性 |
同温同压下,10mL A2气体与20mL B2气体恰好完全反应,生成20mL C气体,则C的化学式应为( )
| A、AB2 |
| B、A2B |
| C、A2B4 |
| D、AB |
下列叙述正确的是( )
| A、48g O3气体含有6.02×1023个O3分子 |
| B、5.6g Fe与足量的稀盐酸反应转移电子0.3 mol |
| C、0.5mol?L-1CuCl2溶液中含有3.01×1023个Cu2+ |
| D、标准状况下,33.6LH2O含有9.03×1023个H2O分子 |
将c(H+)相同的盐酸和醋酸,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的c(H+)仍相同,则m和n的关系是( )
| A、m>n | B、m<n |
| C、m=n | D、不能确定 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、CH3COOH |
| B、Cl2 |
| C、NH4NO3 |
| D、SO2 |
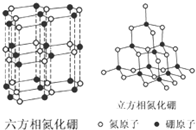 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )| A、立方相氮化硼含配位键B→N |
| B、六方相氮化硼层间作用力小,所以质地软,熔点低 |
| C、两种氮化硼都属于原子晶体 |
| D、六方相氮化硼晶体其结构与石墨相似却不导电,原因是没有可以自由移动的电子 |