题目内容
已知CO和CO2的混合气体质量为14.4g,在标准状况下体积为8.96L,求:
(1)该混和气体的平均摩尔质量(
) ;
(2)CO与CO2的物质的量之比为 ;
(3)将气体全部燃烧成CO2,还需 克O2.
(1)该混和气体的平均摩尔质量(
. |
| M |
(2)CO与CO2的物质的量之比为
(3)将气体全部燃烧成CO2,还需
考点:物质的量的相关计算,摩尔质量
专题:阿伏加德罗常数和阿伏加德罗定律
分析:混合气体的体积为8.96L,则物质的量为
=0.4mol,根据气体的总质量和总物质的量列方程式计算.
| 8.96L |
| 22.4L/mol |
解答:
解:混合气体的体积为8.96L,则物质的量为
=0.4mol,
设混合气体中CO的物质的量为xmol,CO2的物质的量为ymol,则
解之得:
(1)
=
=36 g/mol,故答案为:36 g/mol;
(2)CO与CO2的物质的量之比为0.2mol:0.2mol=1:1,故答案为:1:1;
(3)将气体全部燃烧,发生2CO+O2=2CO2,由方程式可知需要0.1molO2,质量为0.1mol×32g/mol=3.2g,故答案为:3.2.
| 8.96L |
| 22.4L/mol |
设混合气体中CO的物质的量为xmol,CO2的物质的量为ymol,则
|
解之得:
|
(1)
. |
| M |
| 14.4g |
| 0.4mol |
(2)CO与CO2的物质的量之比为0.2mol:0.2mol=1:1,故答案为:1:1;
(3)将气体全部燃烧,发生2CO+O2=2CO2,由方程式可知需要0.1molO2,质量为0.1mol×32g/mol=3.2g,故答案为:3.2.
点评:本题考查物质的量的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度不大,注意从守恒的角度解答.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、氨气通入醋酸溶液:CH3COOH+NH3═CH3COONH4 |
| B、亚硫酸氢钠溶液呈酸性:HSO3-+H2O?H3O++SO32- |
| C、氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| D、稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O |
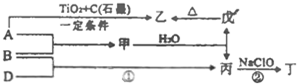 已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).
已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).