题目内容
铜锰氧化物(CuMnO4)可以在常温下催化氧化空气中的一氧化碳和甲醛,因而对新装修的住房有益.
(1)基态Cu2+的电子排布式为 .
(2)甲醛(HCHO)中C原子的杂化方式为 ,它的空间构型为 ,1mol甲醛分子中含 molσ键.
(3)CO常与金属形成羰基化合物,Fe(CO)5的结构示意图是 ;与CO互为等电子体的分子、离子分别是 、 .
(1)基态Cu2+的电子排布式为
(2)甲醛(HCHO)中C原子的杂化方式为
(3)CO常与金属形成羰基化合物,Fe(CO)5的结构示意图是
考点:原子核外电子排布,判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:
分析:(1)根据Cu的电子排布式书写Cu2+离子的电子排布式,注意原子形成离子先失去高能层中高能级电子;
(2)用甲醛中的成键来分析碳原子的杂化类型;利用杂化类型来分析空间结构,并利用判断σ键的规律来分析σ键数目;
(3)Fe(CO)5的结构示意图是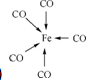 ;原子数电子数相等的微粒叫等电子体;
;原子数电子数相等的微粒叫等电子体;
(2)用甲醛中的成键来分析碳原子的杂化类型;利用杂化类型来分析空间结构,并利用判断σ键的规律来分析σ键数目;
(3)Fe(CO)5的结构示意图是
 ;原子数电子数相等的微粒叫等电子体;
;原子数电子数相等的微粒叫等电子体;解答:
解:(1)Cu是29号元素,原子核外电子数为29,基态原子核外电子排布式为:1s22s22p63s23p63d104s1,铜原子失去4s及3d上各一个电子形成Cu2+,故Cu2+离子的电子排布式为:1s22s22p63s23p63d9,故答案为:1s22s22p63s23p63d9;
(2)甲醛分子中含有碳氧双键,共有3个σ键,则碳原子轨道的杂化类型为sp2杂化,因甲醛中碳原子采取sp2杂化,则分子的空间构型为平面三角形;1mol甲醛分子中含有2mol碳氢σ键,1mol碳氧σ键,故1mol甲醛分子中含3molσ键;故答案为:sp2杂化;
平面三角形;3;
(3)Fe(CO)5的结构示意图是 ;等电子体中原子数和价电子数都相同,则 N2、CN-、CO的原子数都是2,价电子数都是10,则互为等电子体,
;等电子体中原子数和价电子数都相同,则 N2、CN-、CO的原子数都是2,价电子数都是10,则互为等电子体,
故答案为: ;N2;CN-.
;N2;CN-.
(2)甲醛分子中含有碳氧双键,共有3个σ键,则碳原子轨道的杂化类型为sp2杂化,因甲醛中碳原子采取sp2杂化,则分子的空间构型为平面三角形;1mol甲醛分子中含有2mol碳氢σ键,1mol碳氧σ键,故1mol甲醛分子中含3molσ键;故答案为:sp2杂化;
平面三角形;3;
(3)Fe(CO)5的结构示意图是
 ;等电子体中原子数和价电子数都相同,则 N2、CN-、CO的原子数都是2,价电子数都是10,则互为等电子体,
;等电子体中原子数和价电子数都相同,则 N2、CN-、CO的原子数都是2,价电子数都是10,则互为等电子体,故答案为:
 ;N2;CN-.
;N2;CN-.
点评:本题主要考查核外电子排布式、等电子体原理、杂化轨道、共价键类型、分子的平面构型,注重了对物质结构中常考考点的综合,比较容易.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
 SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )
SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )| A、Cu和浓硝酸 |
| B、大理石和稀盐酸 |
| C、CaO和浓氨水 |
| D、高锰酸钾溶液和浓盐酸 |
 用图中的装置Ⅰ通电10分钟后,去掉直流电源,连接成装置Ⅱ,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升,下列说法正确的是( )
用图中的装置Ⅰ通电10分钟后,去掉直流电源,连接成装置Ⅱ,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升,下列说法正确的是( )| A、用装置Ⅱ进行实验时铁电极的电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
| B、用装置Ⅱ进行实验时石墨电极的电极反应为:2H++2e-=H2↑ |
| C、同温、同压下,装置I中石墨电极上方得到的气体比铁电极上方得到的气体多 |
| D、装置Ⅰ通电10分钟后铁电极周围溶液pH降低 |
X、Y、Z、W、M均为短周期元素,X、Y同主族,X的常见氢化物和最高价氧化物的水化物能反应生成一种离子化合物;Z、W、M是第三周期原子序数连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述正确的是( )
| A、X、M两元素的简单气态氢化物的稳定性:X<M |
| B、X、Y、M的最高价氧化物的水化物的酸性:X>Y>M |
| C、Z、W的单质均可在冷的浓硝酸中钝化 |
| D、Z、W、M 的单质均能与NaOH溶液反应 |
 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A、⑥、⑧、⑨对应单核离子的半径依次增大 |
| B、⑤的三种核素的化学性质不相同 |
| C、④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物 |
| D、⑧、⑨两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 |
下列有关化学用语表示正确的是( )
A、NH4Br的电子式: | ||
B、S原子的结构示意图: | ||
| C、乙醇的结构简式:C2H6O | ||
D、原子核内有18个中子的氯原子:
|

 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了