题目内容
10.下列物质含有共价键的是( )| A. | KCl | B. | MgO | C. | H2O | D. | Na2O |
分析 一般金属元素与非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A.KCl中只有离子键,故A不选;
B.MgO中只有离子键,故B不选;
C.H2O中只有H-O共价键,故C选;
D.Na2O中存在离子键,故D不选;
故选C.
点评 本题考查化学键,明确化学键判断的一般规律即可解答,注意铵盐、氯化铝中的化学键为特例,题目难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
10.书法离不开文房四宝(笔、墨、纸、砚),做笔用的狼毫,研墨用的墨条以及宣纸(即白纸)和做砚台用的砚石的主要成分依次是( )
| A. | 蛋白质、炭黑、多糖、无机盐 | B. | 塑料、煤炭、多糖、无机盐 | ||
| C. | 多糖、炭黑、蛋白质、无机盐 | D. | 蛋白质、煤炭、多糖、有机玻璃 |
18.资料显示“O2的氧化性随溶液pH的增大逐渐减弱”.某兴趣小组探究不同条件下KI与O2的反应.实验如下.
(1)实验②中生成I2的离子方程式是4I-+O2+4H+=2I2+2H2O.
(2)实验③的目的是验证Cl-是否影响KI与O2的反应.
(3)实验④比②溶液颜色浅的原因是其他条件相同时,CH3COOH是弱电解质,溶液中c(H+)较盐酸小,O2的氧化性减弱.
(4)为进一步探究KI与O2的反应,用上表中的装置继续进行实验:
I.对于实验⑥的现象.甲同学提出猜想“pH=10时O2不能氧化I-”,设计了下列装置进行实验,验证猜想.
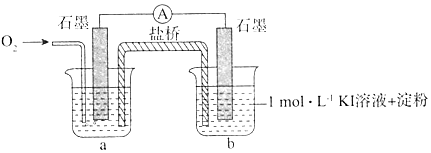
i.烧杯a中的溶液为pH=10的KOH溶液.
ii.实验结果表明,此猜想不成立.支持该结论的实验现象是:通入O2后,电流表指针偏转,烧杯b的溶液颜色变深.
Ⅱ.乙同学向pH=10的KOH溶液(含淀粉)中滴加碘水,溶液先变蓝后迅速褪色.经检测褪色后的溶液中含有IO3-,褪色的原因是(用离子方程式表示)3I2+6OH-=IO3-+5I-+3H2O.
(5)该小组同学对实验过程进行了整体反恩.推测实验①的现象产生的原因可能是中性条件下,O2的氧化性比较弱,该反应速率慢,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;实验⑥的现象产生的原因可能是pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-.
| 装置 | 烧杯中的液体 | 现象(5分钟后) |
 | ①2mL1mol/LKl溶液+5滴淀粉 | 无明显变化 |
| ②2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L HCl | 溶液变蓝 | |
| ③2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L KCl | 无明显变化 | |
| ④2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L CH3COOH | 溶液变蓝,颜色较②浅 |
(2)实验③的目的是验证Cl-是否影响KI与O2的反应.
(3)实验④比②溶液颜色浅的原因是其他条件相同时,CH3COOH是弱电解质,溶液中c(H+)较盐酸小,O2的氧化性减弱.
(4)为进一步探究KI与O2的反应,用上表中的装置继续进行实验:
| 烧杯中的液体 | 现象(5小时后) |
| ⑤2mLpH=8.5混有KOH的1mol/L KI溶液+5滴淀粉 | 溶液才略变蓝 |
| ⑥2mLpH=10混有KOH的1mol/L KI溶液+5滴淀粉 | 无明显变化 |

i.烧杯a中的溶液为pH=10的KOH溶液.
ii.实验结果表明,此猜想不成立.支持该结论的实验现象是:通入O2后,电流表指针偏转,烧杯b的溶液颜色变深.
Ⅱ.乙同学向pH=10的KOH溶液(含淀粉)中滴加碘水,溶液先变蓝后迅速褪色.经检测褪色后的溶液中含有IO3-,褪色的原因是(用离子方程式表示)3I2+6OH-=IO3-+5I-+3H2O.
(5)该小组同学对实验过程进行了整体反恩.推测实验①的现象产生的原因可能是中性条件下,O2的氧化性比较弱,该反应速率慢,短时间内难以生成“一定量”碘单质使溶液颜色发生变化;实验⑥的现象产生的原因可能是pH=10的KOH溶液中I-被氧化生成I2,I2迅速发生歧化反应变为IO3-和I-.
5.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1L1mol•L-1的FeCl3溶液中Fe3+的数目为NA | |
| B. | 32g甲烷中含有2NA个C-H键 | |
| C. | 1molNH2-含有10NA个电子 | |
| D. | 1molNa2O2与足量CO2反应.转移电子数为2NA |
15.有关元素周期表中 34 号元素说法中正确的是( )
| A. | 该元素在人体内具有抗氧化、增强免疫力等功效 | |
| B. | 元素符号为 Sn | |
| C. | 在元素周期表中位于第四周期第ⅣA 族 | |
| D. | 属于金属元素 |
2.下列化学用语正确的是( )
| A. | 聚丙烯的结构简式为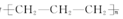 | B. | 丙烷分子的比例模型为 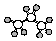 | ||
| C. | 四氯化碳分子的电子式为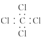 | D. | 2-乙基-1,3-丁二烯的键线式: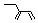 |
19.一杯珍珠奶茶应由三部分组成:糖、奶、茶.奶精(原料是氢化植物油)、奶茶粉放得多,珍珠奶茶的口感就好,成本也高,如果降低成本,可在其中添加白糖或其他香精、奶粉.下列说法正确的是( )
| A. | 奶精能使溴水和酸性KMnO4溶液褪色,其原理相同 | |
| B. | 氢化植物油在稀H2SO4和NaOH溶液中发生水解,所得产物相同 | |
| C. | 白砂糖在人体内水解转化为果糖而被人体吸收 | |
| D. | 奶粉可作为人体所需的一种营养物质 |