题目内容
可按下面方法测定工业甲醇中CH3OH的质量分数:取0.1000g工业甲醇样品,以适量浓H2SO4溶液酸化后,加入20.00mL0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L的(NH4)2Fe(SO4)2标准液滴定,耗去此标准溶液20.00mL时,刚好达到滴定终点.已知上述反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O,Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,求此工业甲醇中CH3OH的质量分数.
考点:溶液中溶质的质量分数及相关计算
专题:计算题
分析:依据化学方程式的定量计算分析,依据FeSO4的消耗量,计算出多余的K2Cr2O7,计算与甲醇反应的K2Cr2O;结合化学方程式进行计算:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O.
解答:
解:由反应②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O可知,反应①剩余的n(Cr2O72-)=
n(Fe2+)=
×0.3000mol/L×20.00mL=0.001mol,
反应①CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O消耗的n(Cr2O72-)=0.2000mol/L×20.00mL-0.001 mol=0.003mol,
则:n(CH3OH)=0.003 mol,w(CH3OH)=
×100%=96%,
答:甲醇中CH3OH的质量分数为96.00%.
| 1 |
| 6 |
| 1 |
| 6 |
反应①CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O消耗的n(Cr2O72-)=0.2000mol/L×20.00mL-0.001 mol=0.003mol,
则:n(CH3OH)=0.003 mol,w(CH3OH)=
| 0.003mol×32g?mol-1 |
| 0.1g |
答:甲醇中CH3OH的质量分数为96.00%.
点评:本题考查了氧化还原反应的化学方程式的综合计算,理顺关系式是解答的关键,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
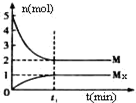 E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g)?Mx(g),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )
E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g)?Mx(g),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )| A、该反应的化学方程式是2HF?(HF)2 | ||
B、t1时刻,保持温度不变,再充入1molM,重新达到平衡时,
| ||
| C、平衡时混合气体的平均摩尔质量是33.3 | ||
| D、M的沸点比同主族下一周期元素的气态氢化物沸点低 |
下表给出几种氯化物的熔点和沸点(*表示在2.5×1.01×105 Pa下测定):
下列有关叙述,不正确的是( )
| NaCl | MgCl2 | AlCl3 | SiCl4 | |
| 熔点(℃) | 801 | 714 | 190* | -68 |
| 沸点(℃) | 1465 | 1418 | 180 | 57 |
| A、AlCl3在加热时升华 |
| B、SiCl4晶体属于分子晶体 |
| C、1500℃时NaCl存在气态分子 |
| D、AlCl3晶体是典型的离子晶体 |
下列关于Na和Na+的叙述中正确的是( )
| A、它们相差一个电子层 |
| B、它们都能与水反应 |
| C、钠原子、钠离子均为同一元素,因此是同种微粒 |
| D、灼烧时,它们的焰色反应都呈紫色 |
日本福岛核事故释放的人工放射性碘
I,半衰期为8.3天,该同位素原子核内的中子数与核外电子数之差是( )
131 53 |
| A、25 | B、78 | C、53 | D、131 |
在浓度均为3mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体质量之比为3:4.则加入铁粉的质量是( )
| A、11.2 g |
| B、8.4 g |
| C、5.6 g |
| D、1.8 g |