题目内容
7.找出合适的序号填在对应的空格中①正戊烷和异戊烷②${\;}_{92}^{235}$U和${\;}_{92}^{238}$U③CH3CH2CH3和 (CH3)2CHCH2CH3④
 和
和 ⑤
⑤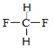 和
和
互为同系物的是③;
属于同一物质的是④⑤;
互为同位素的是②;
互为同分异构体的是①.
分析 同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同官能团的化合物;
组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同;
质子数相同,质量数(或中子数)不同的原子互称同位素;
具有相同分子式而结构不同的化合物互为同分异构体.
解答 解:(1)③CH3CH2CH3和 (CH3)2CHCH2CH3结构相似、通式相同,相差2个CH2原子团,互为同系物,
故答案为:③;
(2)④ 和
和 、⑤
、⑤ 和
和 的分子组成、结构一样,属于同一种物质,
的分子组成、结构一样,属于同一种物质,
故答案为:④⑤;
(3)②${\;}_{92}^{235}$U和${\;}_{92}^{238}$U的质子数都为92,中子数不同,是U元素的不同原子,互为同位素,
故答案为:②;
(4)①正戊烷和异戊烷为分子式相同、结构不同的化合物,二者互为同分异构体,
故答案为:①.
点评 本题考查了同位素、同分异构体、同系物、同素异形体的概念及判断,题目难度不大,注意掌握“五同”的概念及区别,试题侧重基础知识的考查,有利于培养学生的灵活应用能力.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
17. 由硼和镁两种元素组成化合物可为超导材料,如图为该化合物的晶体结构单元示意图:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内.则该化合物的化学式可表示为.( )
由硼和镁两种元素组成化合物可为超导材料,如图为该化合物的晶体结构单元示意图:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内.则该化合物的化学式可表示为.( )
 由硼和镁两种元素组成化合物可为超导材料,如图为该化合物的晶体结构单元示意图:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内.则该化合物的化学式可表示为.( )
由硼和镁两种元素组成化合物可为超导材料,如图为该化合物的晶体结构单元示意图:镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内.则该化合物的化学式可表示为.( )| A. | Mg5B12 | B. | MgB2 | C. | Mg2B | D. | Mg3B2 |
18.短周期元素W、X、Y、Z 的原子序数依次增大,W的单质是空气中体积分数最大的气体,W与Y原子的最外层电子数之和等于X原子的最外层电子数,X、Y、Z简单离子的电子层结构相同,Z原子的最外层电子数等于最内层电子数.下列说法正确的是( )
| A. | 单质的沸点:Z>X>W | |
| B. | 原子半径:Z>Y>X>W | |
| C. | WX与ZX中的化学键类型相同 | |
| D. | 当W的化合价为+4时,W与X只能形成一种化合物 |
15.下列比较正确的是( )
| A. | 沸点:HF>H2O>NH3 | B. | 金属性:Mg>Ca>Ba | ||
| C. | 热稳定性:HBr>HCl>HF | D. | 酸性:HClO4>H2CO3>HClO |
2.下列说法中不正确的是( )
| A. | 通常情况下,镀锌铁的镀层损坏后,仍然可以保护铁不被腐蚀 | |
| B. | 电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极 | |
| C. | 化学电池是将化学能变成电能的装置,它包括一次电池、二次电池和燃料电池等几大类 | |
| D. | 粗铜精炼的过程中,用纯铜板作阳极,粗铜板作阴极 |
12.下列属于非电解质的是( )
| A. | 铜片 | B. | 水 | C. | 酒精 | D. | 食盐 |
19.下列说法不正确的是( )
| A. | 用药匙取用少量二氧化锰粉末 | |
| B. | 蒸馏实验中忘记加沸石,应先停止加热,待溶液冷却后加入沸石,继续蒸馏 | |
| C. | 用干燥洁净的玻璃棒蘸取84消毒液(主成分NaClO),点滴到干的pH试纸上测pH | |
| D. | 油脂制肥皂实验中加乙醇的目的是增大油脂的溶解度,从而增大与氢氧化钠溶液的接触面积,加快油脂皂化反应速率 |
3. 金属钒(V)广泛应用于航空、化工、能源等行业.
金属钒(V)广泛应用于航空、化工、能源等行业.
(1)钒元素基态原子的电子排布式为1s22s22p63s23p63d34s2{或[Ar]3d34s2},3d能级上的未成对电子数为3.
(2)VCl2溶液与乙二胺(H2N-CH2-CH3-NH4)可形成配离子[V(En)2]2+(En是乙二胺的简写),该配离子中所含非金属元素的电负性由大到小的顺序是N>C>H(用元素符号表示).乙二胺分子中氮原子的杂化轨道类型为sp3,乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键.
(3)LiVH4是一种特殊的还原剂,可将乙酸直接还原成乙醇.CH3COOH和CH3CH2OH分子中σ键数目之比为7:8.
(4)钒能形成多种配合物,钒的两种配合物X、Y的化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来).
则X的配离子为[V(NH3)3Cl]2+,Y的配体是NH3、SO42-.
(5)VO晶体的晶胞结构如图所示,VO晶体中V2+的配位数为6.若该晶胞边长为b nm,则该晶体的密度为$\frac{4×67}{(b×1{0}^{-7})^{3}×{N}_{A}}$(用含b,NA的代数式表示)g•cm-3.
 金属钒(V)广泛应用于航空、化工、能源等行业.
金属钒(V)广泛应用于航空、化工、能源等行业.(1)钒元素基态原子的电子排布式为1s22s22p63s23p63d34s2{或[Ar]3d34s2},3d能级上的未成对电子数为3.
(2)VCl2溶液与乙二胺(H2N-CH2-CH3-NH4)可形成配离子[V(En)2]2+(En是乙二胺的简写),该配离子中所含非金属元素的电负性由大到小的顺序是N>C>H(用元素符号表示).乙二胺分子中氮原子的杂化轨道类型为sp3,乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键.
(3)LiVH4是一种特殊的还原剂,可将乙酸直接还原成乙醇.CH3COOH和CH3CH2OH分子中σ键数目之比为7:8.
(4)钒能形成多种配合物,钒的两种配合物X、Y的化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来).
| X | X | Y | Y | |
| 试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
(5)VO晶体的晶胞结构如图所示,VO晶体中V2+的配位数为6.若该晶胞边长为b nm,则该晶体的密度为$\frac{4×67}{(b×1{0}^{-7})^{3}×{N}_{A}}$(用含b,NA的代数式表示)g•cm-3.
4.如图装置用来检验氯气的部分性质,下列说法不正确的是( )


| A. | 装置A的作用是除去氯气中的水蒸气 | |
| B. | 该实验必须在通风橱中进行 | |
| C. | 装置C中发生的反应为Cl2+2NaOH═NaCl+NaClO+H2O | |
| D. | 装置B的现象是干燥处布条褪色,湿润处布条不褪色 |