题目内容
标准状况下将3.36L硫化氢通入含一定量的氢氧化钠溶液中全部吸收,氢氧化钠也全部反应,然后在低温下小心蒸发,得到不含结晶水的固体10.6g,问所得固体中含有什么物质?其质量各为多少克?
考点:化学方程式的有关计算
专题:计算题
分析:标准状况下将3.36L硫化氢气体的物质的量n=
=
=0.15mol,由于硫化氢被完全吸收,而且氢氧化钠也全部反应,故所得的固体物质可能是Na2S或NaHS或两者的混合物,根据硫原子的守恒和最后所得固体的质量,列方程组即可求解.
| V |
| Vm |
| 3.36L |
| 22.4L/mol |
解答:
解:标准状况下将3.36L硫化氢气体的物质的量n=
=
=0.15mol,由于硫化氢被完全吸收,而且氢氧化钠也全部反应,故所得的固体物质可能是Na2S或NaHS或两者的混合物.
设所得的固体产物中Na2S为Xmol,NaHS为Ymol,根据硫原子的守恒可有:X+Y=0.15mol ①,78X+56Y=10.6g ②
解得X=0.1mol,Y=0.05mol
故Na2S的质量m=nM=0.1mol×78g/mol=7.8g
NaHS的质量m=nM=0.05mol×56g/mol=2.8g
答:所得固体中含Na2S和NaHS,其质量分别为7.8g和2.8g.
| V |
| Vm |
| 3.36L |
| 22.4L/mol |
设所得的固体产物中Na2S为Xmol,NaHS为Ymol,根据硫原子的守恒可有:X+Y=0.15mol ①,78X+56Y=10.6g ②
解得X=0.1mol,Y=0.05mol
故Na2S的质量m=nM=0.1mol×78g/mol=7.8g
NaHS的质量m=nM=0.05mol×56g/mol=2.8g
答:所得固体中含Na2S和NaHS,其质量分别为7.8g和2.8g.
点评:本题考查了物质的量的有关计算,根据原子守恒和质量列式即可求得,难度不大.

练习册系列答案
相关题目
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常用电解精炼法将粗铜提纯.在电解精炼时( )
| A、粗铜接电源负极 |
| B、精铜作阴极 |
| C、杂质都将以单质形式沉积到池底 |
| D、精铜片增重2.56g,电路中通过电子为0.04mol |
“低碳生活”是指生活作息时所耗用能量要减少,从而降低碳(特别是二氧化碳)的排放.下列行为不利于低碳生活的是( )
| A、用大排量的轿车代替公交车出行 |
| B、把白炽灯换成节能灯 |
| C、开发太阳能、水能、风能等新能源 |
| D、自备购物布袋,不用塑料方便袋 |
如图为正丁腈的结构简式,正丁腈为易燃液体,有毒性,下列有关说法正确的是( )
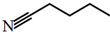

| A、同等条件下,正丁腈在水中的溶解度比在乙醚中的溶解度大 |
| B、其分子式为C4H7N,其密度比水大 |
| C、它还可被命名为氰代丙烷,正丙基氰等,其结构中不含氢键 |
| D、正丁腈由丁烯与氨氧化而得,或由丁醇与氨催化氧化而得 |
下列实验操作正确的是( )
A、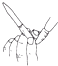 酸式滴定管排气泡 |
B、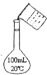 配制100 mL 0.01mol/L盐酸 |
C、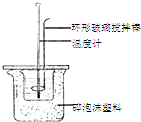 测定中和热 |
D、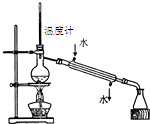 石油的分馏 |
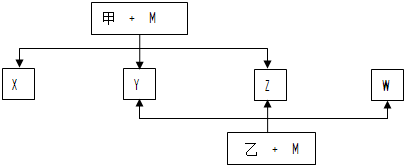
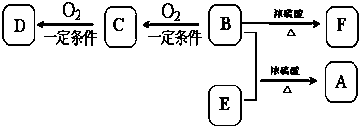
 基团.
基团.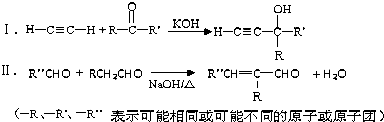
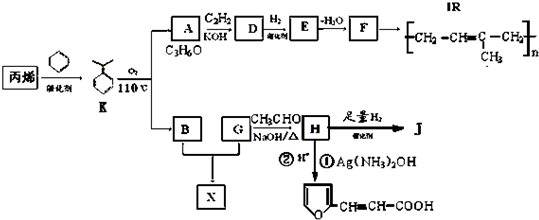
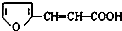 有多种同分异构体,符合下列要求的有
有多种同分异构体,符合下列要求的有