题目内容
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:
2Fe(OH)3+3KClO+4KOH→2K2FeO4+3KCl+5H2O
关于该反应,下列说法正确的是( )
2Fe(OH)3+3KClO+4KOH→2K2FeO4+3KCl+5H2O
关于该反应,下列说法正确的是( )
| A、KClO是还原剂 |
| B、高铁酸钾中铁的化合价为+7 |
| C、每生成1 mol高铁酸钾转移电子3 mol |
| D、高铁酸钾为还原产物 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:2Fe(OH)3+3KClO+4KOH→2K2FeO4+3KCl+5H2O中,Fe元素的化合价由+3价升高为+6价,Cl元素的化合价由+1价降低为-2价,以此来解答.
解答:
解:A.Cl元素的化合价降低,则KClO是氧化剂,故A错误;
B.高铁酸钾中铁的化合价为+6价,故B错误;
C.每生成1 mol高铁酸钾转移电子为1mol×(6-3)=3 mol,故C正确;
D.Fe元素失去电子被氧化,则高铁酸钾为氧化产物,故D错误;
故选C.
B.高铁酸钾中铁的化合价为+6价,故B错误;
C.每生成1 mol高铁酸钾转移电子为1mol×(6-3)=3 mol,故C正确;
D.Fe元素失去电子被氧化,则高铁酸钾为氧化产物,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子数的考查,题目难度不大.

练习册系列答案
相关题目
有下列4种燃料电池的工作原理示意图,其中正极反应的产物为水的是( )
A、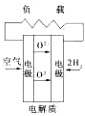 固化氧化物燃料电池 |
B、 碱性氢氧化物电池 |
C、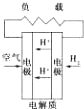 质子交换膜燃料电池 |
D、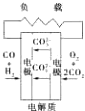 熔融盐燃料电池 |
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法.下列关于“K2SO4”的分类不正确的是( )
| A、正盐 | B、氧化物 |
| C、钾盐 | D、硫酸盐 |
下列叙述中,不正确的是( )
| A、石英可用来制作工艺品 |
| B、硅单质可用来制造太阳能电池 |
| C、硅单质是制造玻璃的主要原料 |
| D、二氧化硅是制造光导纤维的材料 |
下列说法正确的是( )
| A、分子式C7H16的烃,分子中有4个甲基的同分异构体有4种(不考虑立体异构) |
B、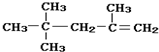 的名称为:2,2,4-三甲基-4-戊烯 的名称为:2,2,4-三甲基-4-戊烯 |
C、化合物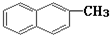 是苯的同系物 是苯的同系物 |
| D、植物油的主要成分是不饱和高级脂肪酸 |
下列变化中,由加成反应引起的是( )
| A、将乙醇蒸汽通过灼热的氧化铜,固体颜色由黑色变为红色 |
| B、苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷 |
| C、一定条件下,将苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D、往溴水中加入四氯化碳溶液,水层褪色 |