题目内容
6. 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1 盐酸测定10mLxmol•L-1氨水.溶液pH随V[(HCl)aq]变化曲线如图所示.下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1 盐酸测定10mLxmol•L-1氨水.溶液pH随V[(HCl)aq]变化曲线如图所示.下列说法正确的是( )| A. | 原氨水浓度x=0.01mol•L-1 | |
| B. | m、p两点溶液中由水电离出来的c(OH-):m>p | |
| C. | n点溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 若在m点溶液中加少量水,[c(NH3•H2O)•c(H+)]/c(NH4+)不变 |
分析 A.由图可知,盐酸和氨水等体积混合,溶液的PH=7,则c(OH-)=c(H+)=1×10-7mol/L,所以c(NH4+)=c(Cl-)=$\frac{1}{2}$×0.01mol/L=0.005mol/L,则c(NH3•H2O)=($\frac{x}{2}$-0.005)mol/L,根据Kb的表达式代入相关数据进行计算;
B.m点为碱溶液,抑制了水的电离,p点溶液为中性,水电离出的c(OH-)=c(H+)=1×10-7mol/L;
C.n点溶液呈碱性,在c(OH-)>c(H+),结合电荷守恒判断;
D.[c(NH3•H2O)•c(H+)]/c(NH4+)为铵根离子的水解平衡常数.
解答 解:A.由图可知,盐酸和氨水等体积混合,溶液的PH=7,则c(OH-)=c(H+)=1×10-7mol/L,所以c(NH4+)=c(Cl-)=$\frac{1}{2}$×0.01mol/L=0.005mol/L,则c(NH3•H2O)=($\frac{x}{2}$-0.005)mol/L,根据Kb=$\frac{0.005×1×1{0}^{-7}}{\frac{x}{2}-0.005}$=1.75×10-5,解得:x=1.006×10-2mol•L-1,故A错误;
B.m点为氨水溶液,铵根离子抑制了水的电离,p点呈中性,水电离出的c(OH-)=c(H+)=1×10-7mol/L,则m、p两点溶液中由水电离出来的c(OH-):m<p,故B错误;
C.n点溶液的pH=9,溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒可知c(NH4+)>c(Cl-),正确的离子浓度大小为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故C错误;
D.在m点溶液中加少量水,由于温度不变,则铵根离子的水解平衡常数K=[c(NH3•H2O)•c(H+)]/c(NH4+)的值不变,故D正确;
故选D.
点评 本题考查溶液酸碱性与溶液pH的关系,题目难度中等,涉及电离平衡常数计算、离子浓度大小比较、水的电离及其影响等知识,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握判断离子浓度大小常用方法,试题培养了学生的分析能力及灵活应用能力.

| A. | 17.9mol•L-1 34.7% | B. | 20.4mol•L-1 33.8% | ||
| C. | 17.9mol•L-1 33.8% | D. | 20.4mol•L-1 34.7% |
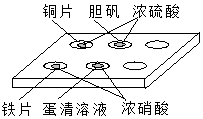 在如图所示的实验中,对点滴板上的现象描述正确的是( )
在如图所示的实验中,对点滴板上的现象描述正确的是( )①装有铜片的孔穴中溶液呈蓝色
②装有胆矾的孔穴中固体的颜色变浅
③装有铁片的孔穴中溶液呈浅绿色
④装有铁片的孔穴中溶液呈浅黄色
⑤装有蛋清溶液的孔穴中呈浅黄色.
| A. | ①④ | B. | ②③ | C. | ①⑤ | D. | ②⑤ |
| A. | “冰,水为之,而寒于水”说明相同质量和温度的水和冰,冰的能量高 | |
| B. | “玉不琢不成器”,“百炼方能成钢”发生的均为化学变化 | |
| C. | “爆竹声中除旧岁,春风送暖入屠苏”爆竹爆炸发生的是分解反应 | |
| D. | “火树银花”中的焰火实质上是金属元素的焰色反应 |
| A. | 加强化石燃料的开采利用,能从根本上解决能源危机 | |
| B. | 苹果放在空气中久置变黄和纸张在空气中久置变黄原理相似 | |
| C. | 从海水中提取物质,都必须经过化学反应才能实现 | |
| D. | 焙制糕点的发酵粉主要成分之一是碳酸氢纳,它也是治疗胃酸过多的一种药剂 |
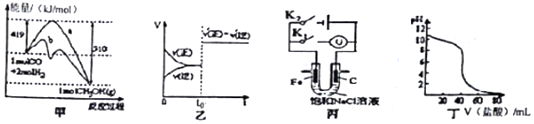
| A. | 图甲表示工业上用CO生成甲醇的反应CO(g)+2H2(g)?CH2OH(g),该反应的△H=-91kJ•mol-1 | |
| B. | 图乙表示已达到平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是加入催化剂 | |
| C. | 图丙中若K1闭合,石墨棒周围溶液pH逐渐升高;若K2闭合,电路中通过0.002NA个电子时,两极理论上共产生0.002mol气体 | |
| D. | 图丁表示盐酸滴加0.1 mol•L-1NaOH溶液的得到的滴定曲线,该实验的指示剂最好选取酚酞 |
| A. | $\frac{a}{A+n}$mol | B. | $\frac{a}{A}$mol | C. | $\frac{(A-N+m)a}{A+m}$mol | D. | $\frac{a}{A}$mol |
| A. | H2(g)+Br2(g)?2HBr(g) | B. | N2(g)+3H2(g)?2NH3(g) | C. | 2SO2(g)+O2(g)?2SO3(g) | D. | C(s)+CO2(g)?2CO(g) |