题目内容
9.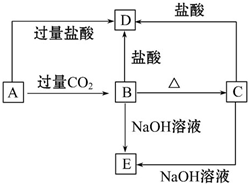 A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,已知A中含钾元素.
A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,已知A中含钾元素.请回答下列问题:
(1)写出化学式:BAl(OH)3,DAlCl3.
(2)五种化合物中难溶于水的是Al(OH)3和A12O3(填化学式).
(3)写出下列反应的离子方程式:
A→B:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
B→E:Al(OH)3+OH-═AlO2-+2H2O,
C→E:Al2O3+2OH-═2AlO2-+H2O.
分析 B、C都既能与盐酸反应又能与NaOH溶液反应,应为两性化合物,因B加热分解可生成C,则可知B为Al(OH)3,C为A12O3,则D为AlCl3,E为NaAlO2,A中含钾元素,A能与二氧化碳反应生成Al(OH)3,则A应为KAlO2,结合对应物质的性质解答该题.
解答 解:(1)通过以上分析知,A、B、C、D、E分别是KAlO2、Al(OH)3、A12O3、AlCl3、NaAlO2,
故答案为:Al(OH)3;AlCl3;
(2)通过以上分析知,A、B、C、D、E分别是KAlO2、Al(OH)3、A12O3、AlCl3、NaAlO2,难溶于水的是Al(OH)3和A12O3,故答案为:Al(OH)3和A12O3;
(3)A→B的反应为AlO2-和Al(OH)3的转化,反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
B→E的反应为Al(OH)3和AlO2-的转化,反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O,
C→E的反应为A12O3和AlO2-的转化,反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;Al(OH)3+OH-═AlO2-+2H2O;Al2O3+2OH-═2AlO2-+H2O.
点评 本题考查了铝及其化合物之间的转化,根据B能和强酸、强碱反应且加热易分解推断知,B是氢氧化铝,再结合物质的反应条件、反应物来分析解答,难度中等,注意偏铝酸根离子和碳酸根离子不能共存,为易错点.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
9.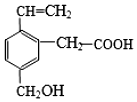 某有机物的结构如图所示,这种有机物不可能具有的性质是( )
某有机物的结构如图所示,这种有机物不可能具有的性质是( )
①可以与氢气发生加成反应;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应; ⑥能发生水解反应.
 某有机物的结构如图所示,这种有机物不可能具有的性质是( )
某有机物的结构如图所示,这种有机物不可能具有的性质是( )①可以与氢气发生加成反应;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应; ⑥能发生水解反应.
| A. | 只有⑥ | B. | ①④ | C. | ⑤⑥ | D. | ④⑥ |
10.下列与生产、生活相关的化学知识描述正确的是( )
| A. | 焚烧废旧塑料以防止“白色污染” | |
| B. | 明矾可用于净水,也可用于淡化海水 | |
| C. | 水瓶胆内部的水垢可用饱和食盐水清洗 | |
| D. | 氢氧燃料电池推广使用可实现碳零排放 |
7.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,1mol羟基含有的电子数为10NA | |
| B. | 将0.5molCl2通入水中,得到的溶液中含有的HClO分子数为0.5NA | |
| C. | 标准状况下,2.24LNO和1.12LO2充分反应,所得气体中原子数目一定为0.3NA | |
| D. | 0.1L1mol•L-1的NaClO溶液中含有的ClO-离子数为0.1NA |
14. 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:
试完成下列问题:
(1)填出图中实验仪器的名称A环形玻璃搅拌棒,B碎泡沫.
(2)实验时用A搅拌溶液的方法是上下搅动.不能用铜丝搅拌棒代替A的理由是铜传热快,防止热量损失.
(3)经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=-56.8kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].
(4)若将HCl溶液改为相同体积、相同浓度的醋酸,测得中和热为△H1=-Q KJ/mol,则Q与57.3的关系为:Q<57.3(填“<”、“>”或“=”),理由是醋酸边反应边电离,醋酸电离吸热.
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和图所示装置进行测定中和热的实验,得到表中的数据:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)填出图中实验仪器的名称A环形玻璃搅拌棒,B碎泡沫.
(2)实验时用A搅拌溶液的方法是上下搅动.不能用铜丝搅拌棒代替A的理由是铜传热快,防止热量损失.
(3)经数据处理,t2-t1=3.4℃.则该实验测得的中和热△H=-56.8kJ/mol[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].
(4)若将HCl溶液改为相同体积、相同浓度的醋酸,测得中和热为△H1=-Q KJ/mol,则Q与57.3的关系为:Q<57.3(填“<”、“>”或“=”),理由是醋酸边反应边电离,醋酸电离吸热.
1.常温下0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是( )
| A. | c(H+) | B. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | C. | c(H+)•c(OH-) | D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$ |
18.下列有关分类的观点正确的是( )
①由苯制取溴苯、硝基苯、环己烷的反应都属于取代反应
②铅蓄电池、锂电池、碱性锌锰电池都属于二次电池
③碳素钢、不锈钢和目前流通的硬币都属于合金
④浓盐酸、浓硫酸、浓硝酸都属于氧化性酸
⑤氨水、醋酸、氢氧化铝都属于弱电解质
⑥豆浆、淀粉水溶液、雾都属于胶体.
①由苯制取溴苯、硝基苯、环己烷的反应都属于取代反应
②铅蓄电池、锂电池、碱性锌锰电池都属于二次电池
③碳素钢、不锈钢和目前流通的硬币都属于合金
④浓盐酸、浓硫酸、浓硝酸都属于氧化性酸
⑤氨水、醋酸、氢氧化铝都属于弱电解质
⑥豆浆、淀粉水溶液、雾都属于胶体.
| A. | ③⑥ | B. | ①④ | C. | ②③⑥ | D. | ②④⑤ |
19.有关氨的说法不正确的( )
| A. | NH3是10电子微粒 | |
| B. | 氨气易液化,液氨可用作制冷剂 | |
| C. | 蘸有浓盐酸的玻璃棒遇氨气产生的白烟 | |
| D. | 氨气是电解质,NH3•H2O是非电解质 |
