题目内容
①已知:0.5mol液态肼(N2H4)与足量的液态双氧水反应生成氮气和水蒸气,放出256kJ的热量,写出该反应的热化学方程式
②此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大优点是 .
②此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大优点是
考点:热化学方程式
专题:化学反应中的能量变化
分析:①根据热化学方程式的书写原则和注意问题写出;注意物质的聚集状态标注,焓变的正负号和单位;
②依据反应产生的物质性质分析判断;
②依据反应产生的物质性质分析判断;
解答:
解:(1)已知0.5mol液态肼和足量双氧水反应生成氮气和水蒸气时放出256KJ的热量;肼和双氧水反应的热化学方程式:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-512KJ/mol,
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-512KJ/mol;
(2)还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,无污染;故答案为:产物为氮气和水,无污染;
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-512KJ/mol;
(2)还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,无污染;故答案为:产物为氮气和水,无污染;
点评:本题考查了热化学方程式的书写方法和注意问题,盖斯定律的应用,热化学方程式的计算,题目较简单.

练习册系列答案
相关题目
化学与生产、生活密切相关.下列叙述中,不正确的是( )
| A、制作计算机芯片的材料是Si晶体,漂白液的有效成分是NaClO |
| B、二氧化碳和氮气均是造成温室效应的气体 |
| C、食醋可去除水垢,NH4Cl溶液可去除铁锈 |
| D、SO2和NO2都能使雨水的pH<5.6,造成酸雨 |
下列反应的离子方程式正确的是( )
| A、向澄清石灰水中滴加盐酸:Ca(OH)2+2H+=Ca2++2H2O |
| B、向铜粉中加入稀H2SO4:Cu+2H+=Cu2++H2↑ |
| C、向CuSO4溶液中加入Fe粉:Fe+Cu2+=Fe2++Cu |
| D、向AgNO3溶液中加入Cu粉:Ag++Cu=Cu2++Ag |
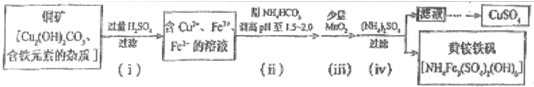
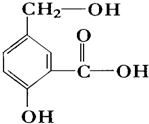 在某有机物A的分子中,具有酚羟基、醇羟基、羟基等官能团,其结构简式如图.
在某有机物A的分子中,具有酚羟基、醇羟基、羟基等官能团,其结构简式如图.
 和
和 