题目内容
6.肉桂酸甲酯由C、H、O三种元素组成,质谱分析其分子的相对分子质量为162,核磁共振氢谱谱图显示有6个峰,其面积之比为1:2:2:1:1:3,利用红外光谱仪检测其中的某些基团,测得红外光谱如图: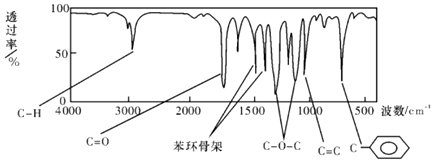
则肉桂酸甲酯的结构简式是
 (不考虑立体异构)
(不考虑立体异构)
分析 根据红外光谱可知肉桂酸甲酯分子中含有双键和酯基,苯环,则其相对分子质量是162,确定分子式,核磁共振氢谱图中有六个吸收峰,峰面积比为1:2:2:1:1:3,说明有6种氢,最后确定结构简式.
解答 解:红外光谱可知肉桂酸甲酯分子中含有双键和酯基,苯环,则其相对分子质量是162,确定分子式为C10H10O2,核磁共振氢谱图中有六个吸收峰,峰面积比为1:2:2:1:1:3,说明有6种氢,其结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物结构简式的推断,题目难度中等,借助于红外光谱和相对分子质量推出分子式是解题的关键,注意掌握常见有机物组成与结构,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
20.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 | |
| B. | 制作航天服的聚脂纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| C. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| D. | 重金属离子能杀死H7N9禽流感病毒 |
14.下列说法不正确的是( )
| A. | 利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液 | |
| B. | 将饱和FeCl3溶液滴入沸水中,将继续煮沸至溶液呈红褐色即生成氢氧化铁胶体 | |
| C. | 用过滤法可以除去Fe(OH)3胶体中的FeCl3 | |
| D. | 用豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质 |
1.铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O═Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
| A. | 电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe | |
| B. | 电池放电时,负极反应为Fe-2e-═Fe2+ | |
| C. | 电池充电过程中,阴极附近溶液的pH升高 | |
| D. | 电池充电时,阳极反应为2Ni(OH)2+2OH--2e-═Ni2O3+3H2O |
15.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+.取该溶液100mL,加入过量NaOH溶液并加热,得到0.02mol气体,同时产生红褐色沉淀;将过滤洗涤后的沉淀灼烧得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.下列说法正确的是( )
| A. | 该溶液中最多存在4种离子 | |
| B. | 该溶液可由KCl、(NH4)2SO4和FeCl3配制而成 | |
| C. | 该溶液中一定存在Cl-、且c(Cl-)≥0.4mol•L-1 | |
| D. | 该溶液中不能确定是否存在CO32- |
16.下列说法正确的是( )
| A. | 摩尔是七个基本物理量之一 | |
| B. | 硫酸钠和水分别属于非电解质和弱电解质 | |
| C. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| D. | 分散系中分散质粒子的直径:Fe(OH)3浊液>Fe(OH)3胶体>FeCl3溶液 |
 .
.