题目内容
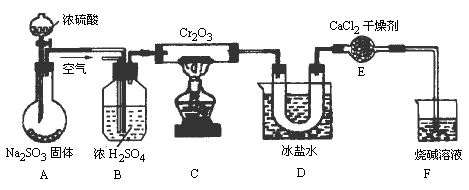
某同学根据2SO2+O2![]() 2SO3+196.6kJ设计如图11-1 实验装置制备SO3固体
2SO3+196.6kJ设计如图11-1 实验装置制备SO3固体
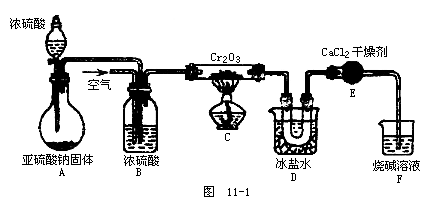
请回答下列问题:
(1)实验前,必须进行的操作是(填操作名称,不必写具体过程)____。</PGN0050B.TXT/PGN>
(2)在A装置中加入亚硫酸钠固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是____。
(3)B装置的三个作用是①____;②____;③____。
(4)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防止温度过高。这样做的原因是____;____。
(5)装置E的作用是____。
解析:

(1)已知1.0mol·L—1NaHSO3溶液的pH为3.5,则此溶液离子浓度从大到小的顺序为 (用离子符号表示)。
 (2)能证明Na2SO3溶液中存在水解平衡SO32-+H2O
(2)能证明Na2SO3溶液中存在水解平衡SO32-+H2O![]() HSO3-+OH-的事实是 (填序号)。
HSO3-+OH-的事实是 (填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,在加入BaCl2溶液后产生沉淀且红色退去
(3)工业上利用催化氧化反应将SO2转化为SO3:2SO2+ O2 ![]() 2SO3。若某温度下,此反应的起始浓度c(SO2)=1.0mol·L—1,c(O2)=1.5mol·L—1,达到平衡后,SO2的转化率为50%,则此温度下该反应的平衡常数K= 。
2SO3。若某温度下,此反应的起始浓度c(SO2)=1.0mol·L—1,c(O2)=1.5mol·L—1,达到平衡后,SO2的转化率为50%,则此温度下该反应的平衡常数K= 。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2IO3-+5SO32-+2H+===I2+5SO42-+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
| 0.01mol·L-1 KIO3 酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1 Na2SO3 溶液的体积/mL | H2O的体积 /mL | 实验 温度 /℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
表中V2=___________mL,该实验的目的是______________ ______。
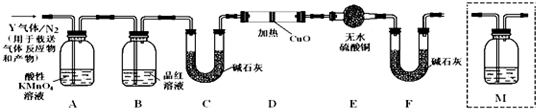
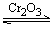 2SO3(放热反应),设计如图所示实验装置制备SO3固体.
2SO3(放热反应),设计如图所示实验装置制备SO3固体.