题目内容
下列表示对应化学反应的离子方程式正确的是
A.向氯化铝溶液通入过量的氨气:Al3+ +4OH- AlO2- +2H2O
AlO2- +2H2O
B.过量氯气通人溴化亚铁溶液中2Cl2 +2Fe2+ +2Br- 4Cl-+2Fe3++ Br2
4Cl-+2Fe3++ Br2
C.次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl—+H2O=Cl2↑+2OH—
D.NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O
D
【解析】
试题分析:A、向氯化铝溶液通入过量的氨气,氢氧化铝不溶于弱碱氨水,应生成氢氧化铝沉淀,错误;B、过量氯气通人溴化亚铁溶液中应为3Cl2 +2Fe2+ +4Br- 6Cl-+2Fe3++ 2Br2,错误;C.次氯酸钠与浓盐酸反应产生Cl2应为:ClO-+Cl—+2H+=Cl2↑+H2O,错误;D、NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O,正确。
6Cl-+2Fe3++ 2Br2,错误;C.次氯酸钠与浓盐酸反应产生Cl2应为:ClO-+Cl—+2H+=Cl2↑+H2O,错误;D、NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O,正确。
考点:考查离子方程式正误判断。

下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向盛有Fe(NO3)2溶液的试管中加入0.1 mol·L-1 H2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
B | 向溶液中先滴加稀盐酸,再滴加BaCl2溶液 | 先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀 | 溶液中一定含有SO42- |
C | 用洁净铂丝蘸取某溶液置于酒精灯火焰上灼烧 | 火焰呈黄色 | 溶液中含Na+,无K+ |
D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y一定是Cl2 |
(12分)已知反应2HI(g)  H2(g) +I2(g)在T℃下的平衡常数为0.01。T℃时,在容积为2L的密闭容器中加入HI ,反应到某时刻测得各组分的浓度如下:
H2(g) +I2(g)在T℃下的平衡常数为0.01。T℃时,在容积为2L的密闭容器中加入HI ,反应到某时刻测得各组分的浓度如下:
物质 | HI | H2 | I2 |
浓度/(mol·L-1) | 0.40 | 0.60 | 0.60 |
请计算回答下列问题(写出计算过程,否则不得分):
(1)起始加入HI的物质的量 mol。
(2)达到平衡后HI的物质的量浓度 mol·L-1(请保留三位有效数字)。
(3)T℃时,在另一个体积一定的密闭容器中,将I2(g)与H2(g) 置于其中发生上述反应,若达到平衡时H2(g)与I2(g)的体积比为1∶4,计算平衡时HI的体积分数为 ,以及开始时H2(g)与I2(g)的体积比为 。
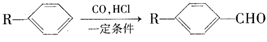
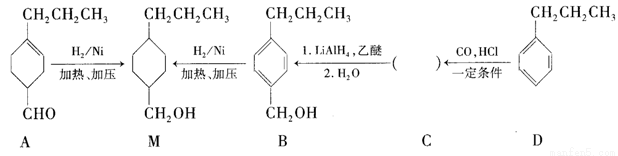
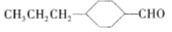 和______(写结构简式)生成。
和______(写结构简式)生成。 CO(g) ΔH=-110.5 kJ·mol-1②Mg(g)+O2(g)
CO(g) ΔH=-110.5 kJ·mol-1②Mg(g)+O2(g) Mg(g)+CO(g),该反应的ΔH= 。
Mg(g)+CO(g),该反应的ΔH= 。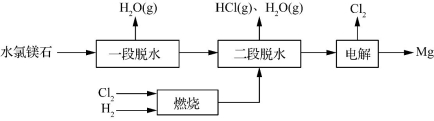
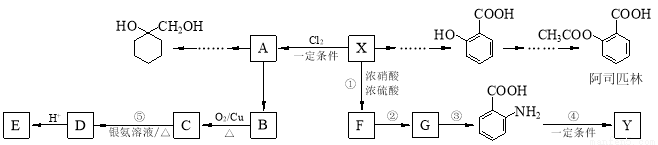

 (苯胺,易被氧化)
(苯胺,易被氧化)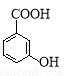 有多种同分异构体, 写出同时符合下列4个条件它的同分异构体的结构简式:
有多种同分异构体, 写出同时符合下列4个条件它的同分异构体的结构简式: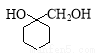 的流程图:
的流程图: 甲
甲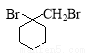
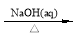
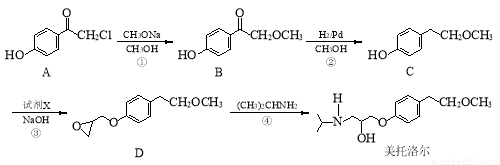
 为原料
为原料 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: CH3CH2Br
CH3CH2Br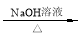 CH3CH2OH
CH3CH2OH