��Ŀ����
��12�֣���ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) ? CH3OH(g)
��1����ͼ��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯���÷�Ӧ�� ������ȡ����ȡ�����Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��
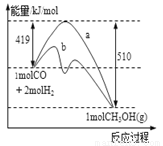
ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȡ�
��2���÷�Ӧƽ�ⳣ��K�ı���ʽΪK= ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������
��3�����������£����д�ʩ����ʹ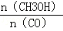 ������� ��
������� ��
a�������¶� b������He�� c���ٳ���1molCO��2molH2 d��ʹ�ô�����
��12�֣���1�� ���� CO��g��+2H2��g��=CH3OH��g����H=��91kJ/mol �� ����
��2��K= ������ ��3�� c ��
������ ��3�� c ��
��������
�����������1�����ڸ÷�Ӧ�ķ�Ӧ���������������������������Է�Ӧ�����������������ͷų�������˸÷�Ӧ�Ƿ��ȷ�Ӧ������ͼʾ�ṩ��������֪�÷�Ӧ���Ȼ�ѧ����ʽ�� CO��g��+2H2��g��=CH3OH��g����H=��91kJ/mol��ѡ�����˵Ĵ���ֻ�ܸı䷴Ӧ;�������ͷ�Ӧ�Ļ�ܣ����Ƿ�Ӧ�Ȳ���ı䣻��2���÷�Ӧƽ�ⳣ��K�ı���ʽΪK= �����ڸ÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����Ը���ƽ���ƶ�ԭ�����¶����ߣ�ƽ�������ȵ��淴Ӧ�����ƶ�������ƽ�ⳣ��K��С����3������������a�������¶ȣ�ƽ�������ƶ���
�����ڸ÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����Ը���ƽ���ƶ�ԭ�����¶����ߣ�ƽ�������ȵ��淴Ӧ�����ƶ�������ƽ�ⳣ��K��С����3������������a�������¶ȣ�ƽ�������ƶ��� ��С������ b������He�����������ʵ�Ũ�Ȳ��䣬����ƽ�ⲻ�ƶ������
��С������ b������He�����������ʵ�Ũ�Ȳ��䣬����ƽ�ⲻ�ƶ������ ���䣬����c���ٳ���1molCO��2molH2 ��ƽ�������ƶ���CH3OH�����ʵ�������
���䣬����c���ٳ���1molCO��2molH2 ��ƽ�������ƶ���CH3OH�����ʵ������� ������ȷ�� d��ʹ�ô���ƽ�ⲻ�����ƶ���
������ȷ�� d��ʹ�ô���ƽ�ⲻ�����ƶ��� ���䣬����
���䣬����
���㣺���鷴Ӧ�����ܵĹ�ϵ���Ȼ�ѧ����ʽ����д����ѧƽ�ⳣ���ı��Ӱ��ƽ���ƶ������ء�

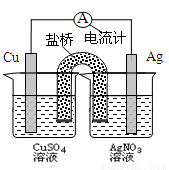
 H2(g)+I2(g)���ֱ��ƽ��ʱ�����¹�ϵ��ȷ����
H2(g)+I2(g)���ֱ��ƽ��ʱ�����¹�ϵ��ȷ����