题目内容
18.(1)写出电解饱和食盐水的化学方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑漂白粉置于空气中变质失效Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO、2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑.
(2)书写物质的电子式:氮气
 ,氯化钙
,氯化钙 ,硫化氢 结构式:H-S-H.以上三种物质中其中属于共价化合物的是H2S,晶体类型为分子晶体.
,硫化氢 结构式:H-S-H.以上三种物质中其中属于共价化合物的是H2S,晶体类型为分子晶体.
分析 (1)电解饱和食盐水生成氢氧化纳、氢气和氯气,漂白粉成分为氯化钙和次氯酸钙的混合物,其中次氯酸钙吸收空气中的二氧化碳和水蒸气反应生成碳酸钙和次氯酸,次氯酸见光分解生成盐酸和氧气;
(2)氮气是氮原子间以三对共用电子对形成三键结构,氯化钙是钙离子和氯离子形成的离子化合物,氯化钙的电子式中,两个氯离子不能合并,氯离子应该分别写在钙离子的两边,硫化氢是硫原子和氢原子形成两对共用电子对形成的共价化合物;分子构成的物质形成分子晶体,离子化合物形成的晶体为离子化合物.
解答 解:(1)电解饱和食盐水生成氢氧化纳、氢气和氯气:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,漂白粉在空气中变质是因为其有效成分次氯酸钙与空气中的二氧化碳反应生成了次氯酸,并且次氯酸见光、受热分解,从而使漂白粉失效,即发生Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑,
故答案为:2C12+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO;2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑.
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑;
(2)氮气分子中两个氮原子共用3对电子,电子式为: ,氯化钙为离子化合物,其电子式中,两个氯离子不能合并,氯化钙正确的电子式为:
,氯化钙为离子化合物,其电子式中,两个氯离子不能合并,氯化钙正确的电子式为: ,硫化氢结构式为H-S-H,其中属于共价化合物的是H2S,形成晶体为分子晶体,
,硫化氢结构式为H-S-H,其中属于共价化合物的是H2S,形成晶体为分子晶体,
故答案为: ,
, ,H2S,分子;.
,H2S,分子;.
点评 本题考查了物质性质和化学方程式书写,物质结构的表示方法,主要是电子式、晶体类型和物质类型的判断,题目难度中等.

| A. | 天津港爆炸案中对剧毒的氰化钠(NaCN) 喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| B. | 碳酸钙分解、氢氧化钡晶体和氯化铵固体反应、高温下铝与氧化铁反应都是吸热反应 | |
| C. | 刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 | |
| D. | 石油原油的脱水,有色玻璃、纳米材料、塑料、橡胶及合成纤维等制造过程都会用到胶体 |
| A. | 用磁铁分离出混合物中的铁粉 | B. | 将混合物溶于二硫化碳后过滤 | ||
| C. | 将混合物溶解于稀盐酸后过滤 | D. | 将混合物加热升华 |
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
| A. | .①②③ | B. | ②③ | C. | ① | D. | 全部 |
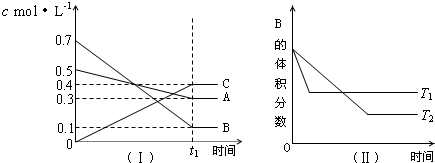
| A. | 在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 | |
| B. | (t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动 | |
| C. | 其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 | |
| D. | 由图(Ⅱ)可知,T1>T2,且该正反应为吸热反应 |
| A. | 铜片溶解,生成物冷却后加水稀释溶液成蓝色 | |
| B. | 生成的气体体积为1.12L | |
| C. | 参加反应的硫酸与被还原的硫酸物质的量之比为2:1 | |
| D. | 该实验中可用NaOH溶液处理尾气 |
①Si ②Al ③Cl ④Fe ⑤Na.
| A. | ①②⑤ | B. | ①② | C. | ①②③ | D. | ①②③④⑤ |
| A. | 向某溶液中滴加KSCN 溶液,溶液呈血红色,证明存在Fe3+ | |
| B. | 氢氧化钠溶液保存在带橡皮塞的试剂瓶中 | |
| C. | 漂白粉常作环境消毒剂 | |
| D. | 工业上用电解饱和食盐水来制取金属钠 |