题目内容
已知反应:
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3,
下列说法正确的是( )
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3,
下列说法正确的是( )
| A、上述三个反应都有单质生成,所以都是置换反应 |
| B、反应③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
| C、反应②中还原剂与氧化剂的物质的量之比为6:1 |
| D、氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:①Cl2+2KBr=2KCl+Br2,Cl元素的化合价降低,Br元素的化合价升高;
②KClO3+6HCl=3Cl2↑+KCl+3H2O,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0;
③2KBrO3+Cl2=Br2+2KClO3,Cl元素的化合价升高,Br元素的化合价降低,以此来解答.
②KClO3+6HCl=3Cl2↑+KCl+3H2O,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0;
③2KBrO3+Cl2=Br2+2KClO3,Cl元素的化合价升高,Br元素的化合价降低,以此来解答.
解答:
解:A.②KClO3+6HCl=3Cl2↑+KCl+3H2O中,反应物不存在单质,不属于置换反应,故A错误;
B.反应③中lmol还原剂(Cl2)反应,由电子守恒可知,氧化剂得到电子的物质的量为1mol×2×(5-0)=10mol,故B错误;
C.反应②中还原剂为HCl,与氧化剂KClO3的物质的量比为5:1,
HCl作酸,故C错误;
D.由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2,故D正确;
故选D.
B.反应③中lmol还原剂(Cl2)反应,由电子守恒可知,氧化剂得到电子的物质的量为1mol×2×(5-0)=10mol,故B错误;
C.反应②中还原剂为HCl,与氧化剂KClO3的物质的量比为5:1,
| 1 |
| 6 |
D.由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2,故D正确;
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应转移电子、氧化性比较的考查,注重规律性知识的应用,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
在一定条件下体积不变的密闭容器中,一定量的混合气体发生反应:aA(g)+bB(g)?cC(g)△H<0,达到平衡时,测得c(B)=0.48mol?L-1.保持温度不变,把容器体积扩大到原来的2倍,使其重新达到平衡,测得c(B)=0.27mol?L-1.下列有关说法不正确的是( )
| A、a+b>c |
| B、A的转化率增大 |
| C、C的体积分数降低 |
| D、平衡一定逆向移动 |
下列物质中属于弱电解质的是( )
| A、CaCO3 |
| B、O2 |
| C、食盐 |
| D、醋酸 |
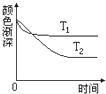 反应:A+B?2C,其中A为有色气体,其混合物颜色深浅与反应时间、温度(T)之间的关系如图所示(B、C均为无色物质).下列说法中不正确的是( )
反应:A+B?2C,其中A为有色气体,其混合物颜色深浅与反应时间、温度(T)之间的关系如图所示(B、C均为无色物质).下列说法中不正确的是( )| A、T1>T2,该反应是放热反应 |
| B、若A、B、C均为气态物质,增大压强时B的转化率不变 |
| C、若A、B、C均为气态物质时,增大压强,混合气体的颜色不变 |
| D、若A、B为气体,C为固体,增大压强时A的转化率增大 |
符合下列某一个选项的反应一定可以自发进行,这个选项是( )
| A、吸热的熵增反应 |
| B、放热的熵增反应 |
| C、放热的熵减反应 |
| D、吸热的熵减反应 |
下列叙述与盐类水解无关的是( )
| A、热纯碱溶液去污能力强 |
| B、明矾可作净水剂 |
| C、Al3+和HCO3-在溶液中不能大量共存 |
| D、配FeCl2溶液加铁粉 |
在甲、乙两个密闭容器中,分别充入HI、NO2,发生反应:(甲)2HI(g)?H2(g)+I2(g)△H>0,(乙)2NO2(g)?N2O4(g)△H<0.下列措施能使两个容器中混合气体颜色均加深且平衡发生移动的是( )
| A、增大反应物浓度 |
| B、增大压强(减小体积) |
| C、降温 |
| D、加催化剂 |
下列溶液与铝不能发生反应产生氢气的是( )
| A、盐酸溶液 |
| B、氢氧化钠溶液 |
| C、氯化铵溶液 |
| D、硫酸钠溶液 |
 “神九”飞船的发射成功,标志着我国航天事业进入领先行业.
“神九”飞船的发射成功,标志着我国航天事业进入领先行业.