题目内容
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L,下列措施中能够减少SO2排放量的是( )
①用天然气代替煤炭作民用燃料
②使用水煤气或干馏煤气作燃料
③循环处理吸收塔放出的尾气
④将块状煤粉碎,提高其燃烧效率.
①用天然气代替煤炭作民用燃料
②使用水煤气或干馏煤气作燃料
③循环处理吸收塔放出的尾气
④将块状煤粉碎,提高其燃烧效率.
| A、①②③ | B、①③④ |
| C、①②④ | D、①②③④ |
考点:二氧化硫的污染及治理
专题:
分析:①煤炭中含有一定量的硫,用煤炭作民用燃料会向大气中排放出较多的SO2;
②水煤气的主要成分为一氧化碳和氢气、干馏煤气主要成分为烃的混合物,都不含硫;
③循环处理吸收塔放出的尾气,可以提高二氧化硫的转化率;
④将块状煤粉碎,提高其燃烧速率,但不能减少硫的排放.
②水煤气的主要成分为一氧化碳和氢气、干馏煤气主要成分为烃的混合物,都不含硫;
③循环处理吸收塔放出的尾气,可以提高二氧化硫的转化率;
④将块状煤粉碎,提高其燃烧速率,但不能减少硫的排放.
解答:
解:①民用煤中含有S元素,天然气不含S,用天然气代替煤炭作民用燃料,所以能减少SO2排放量,故①正确;
②煤可与水蒸气反应制成水煤气,其反应方程为:C+H2O(g)
CO+H2,所以水煤气的主要成分是CO和H2,干馏煤是在隔绝空气的条件下,将煤加热到900~1100℃时,可以得到焦炭、煤焦油、煤气等物质,干馏煤气成分为烃的混合物,水煤气和干馏煤气都不含硫,所以能减少SO2排放,故②正确;
③通过循环处理吸收塔放出的尾气,可以增大二氧化硫的转化率,大大减小了SO2排放量,故③正确;
④将块状煤粉碎,能加快煤和氧气的接触面积,提高燃烧的速率,但不能除掉其中的硫,所以无法减少二氧化硫的排放量,故④错误;
根据以上分析可知,能够简单二氧化硫排放量的为:①②③,
故选A.
②煤可与水蒸气反应制成水煤气,其反应方程为:C+H2O(g)
| ||
③通过循环处理吸收塔放出的尾气,可以增大二氧化硫的转化率,大大减小了SO2排放量,故③正确;
④将块状煤粉碎,能加快煤和氧气的接触面积,提高燃烧的速率,但不能除掉其中的硫,所以无法减少二氧化硫的排放量,故④错误;
根据以上分析可知,能够简单二氧化硫排放量的为:①②③,
故选A.
点评:本题考查了二氧化硫性质应用,主要考查污染气体的处理与防治,题目难度不大,注意掌握二氧化碳的化学性质,要明确二氧化硫对大气的污染及治理措施.

练习册系列答案
相关题目
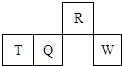 短周期元素R、T、Q、W在元素周期标准的相对位置如图所示,其中T所处的周期序数和族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期标准的相对位置如图所示,其中T所处的周期序数和族序数相等.下列判断不正确的是( )| A、R的简单气态氢化物可以使湿润红色石蕊试纸变蓝 |
| B、W的最高价氧化物的水化物是一种强酸 |
| C、Q的最高价氧化物难溶于水 |
| D、T最高价氧化物的水化物是一种强碱 |
下列说法正确的是( )
| A、向50 mL 1mol?L-1的盐酸中加入烧碱后,水的Kw不变 | ||
| B、NH4C1和NH3?H2O混合液中,二者对对方的平衡都起了抑制作用 | ||
| C、室温时某溶液的pH<7,则该物质一定是酸或强酸弱碱盐 | ||
D、常温下0.1 mol?L-1的HA溶液中
|
向NaBr和NaI的混合溶液中通入一定量Cl2后,将溶液蒸干并灼烧,最后得到的物质不可能是( )
| A、NaCl |
| B、NaCl、NaBr、NaI |
| C、NaCl、NaBr |
| D、NaCl、NaI |

 如图所示的装置中,A、B均为石墨电极.回答下列问题:
如图所示的装置中,A、B均为石墨电极.回答下列问题:
