题目内容
写出下列反应式,并作简要回答:(1)写化学方程式:
①呼吸面具中CO2与过氧化钠反应:______.
②工业生产漂白粉:______ CaCl2+Ca(ClO)2+2H2O
【答案】分析:(1)①过氧化钠可以和二氧化碳反应生成氧气,可做供氧剂;
②氯气属于酸性气体,能和碱反应;
③浓硫酸具有强氧化性,能将单质碳氧化;
(2)①金属铝既能和强碱反应又能和强酸反应,均产生氢气;
②二氧化硅是酸性氧化物,能和氢氧化钠反应;
③硝酸具有氧化性,能和大多数的金属反应.
解答:解:(1)①过氧化钠可以和二氧化碳反应生成碳酸钠和氧气,即2Na2O2+2CO2═2Na2CO3+O2↑,
故答案为:2Na2O2+2CO2═2Na2CO3+O2↑;
②工业上将氯气通到石灰乳中来生产漂白粉,原理是:2Cl2+2Ca(OH)2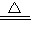 CaCl2+Ca(ClO)2+2H2O,
CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2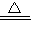 CaCl2+Ca(ClO)2+2H2O;
CaCl2+Ca(ClO)2+2H2O;
③浓硫酸具有强氧化性,能和非金属单质碳加热时反应,即C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O,化合价降低的元素是硫酸中的硫元素,对应的产物是二氧化硫,所以H2SO4是氧化剂,SO2是还原产物,
故答案为:C+2H2SO4(浓)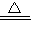 CO2↑+2SO2↑+2H2O;H2SO4;SO2;
CO2↑+2SO2↑+2H2O;H2SO4;SO2;
(2)①金属铝能和烧碱反应生成氢气,实质是:2Al+2OH-+2H2O═2 AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O═2 AlO2-+3H2↑;
②二氧化硅是酸性氧化物,能和氢氧化钠反应生成盐和水,即SiO2+2OH-═SiO32-+H2O,
故答案为:SiO2+2OH-═SiO32-+H2O;
③硝酸具有氧化性,稀硝酸对应的还原产物是一氧化氮,反应实质为:2NO3-+3Cu+8H+═3Cu2++2NO↑+4H2O,反应中有8mol的硝酸参加反应,只有2mol的硝酸做氧化剂被还原,反应转移电子为6mol,
故答案为:2NO3-+3Cu+8H+═3Cu2++2NO↑+4H2O;6.
点评:本题考查学生化学方程式和离子方程式的书写知识,要熟记教材知识,可以根据所学知识进行回答,难度不大.
②氯气属于酸性气体,能和碱反应;
③浓硫酸具有强氧化性,能将单质碳氧化;
(2)①金属铝既能和强碱反应又能和强酸反应,均产生氢气;
②二氧化硅是酸性氧化物,能和氢氧化钠反应;
③硝酸具有氧化性,能和大多数的金属反应.
解答:解:(1)①过氧化钠可以和二氧化碳反应生成碳酸钠和氧气,即2Na2O2+2CO2═2Na2CO3+O2↑,
故答案为:2Na2O2+2CO2═2Na2CO3+O2↑;
②工业上将氯气通到石灰乳中来生产漂白粉,原理是:2Cl2+2Ca(OH)2
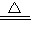 CaCl2+Ca(ClO)2+2H2O,
CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2
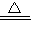 CaCl2+Ca(ClO)2+2H2O;
CaCl2+Ca(ClO)2+2H2O;③浓硫酸具有强氧化性,能和非金属单质碳加热时反应,即C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O,化合价降低的元素是硫酸中的硫元素,对应的产物是二氧化硫,所以H2SO4是氧化剂,SO2是还原产物,
故答案为:C+2H2SO4(浓)
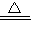 CO2↑+2SO2↑+2H2O;H2SO4;SO2;
CO2↑+2SO2↑+2H2O;H2SO4;SO2;(2)①金属铝能和烧碱反应生成氢气,实质是:2Al+2OH-+2H2O═2 AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O═2 AlO2-+3H2↑;
②二氧化硅是酸性氧化物,能和氢氧化钠反应生成盐和水,即SiO2+2OH-═SiO32-+H2O,
故答案为:SiO2+2OH-═SiO32-+H2O;
③硝酸具有氧化性,稀硝酸对应的还原产物是一氧化氮,反应实质为:2NO3-+3Cu+8H+═3Cu2++2NO↑+4H2O,反应中有8mol的硝酸参加反应,只有2mol的硝酸做氧化剂被还原,反应转移电子为6mol,
故答案为:2NO3-+3Cu+8H+═3Cu2++2NO↑+4H2O;6.
点评:本题考查学生化学方程式和离子方程式的书写知识,要熟记教材知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目