题目内容
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中铜片是正极,乙中铜片是负极 |
| C、两烧杯中溶液的酸性均减弱 |
| D、产生气泡的速度甲比乙慢 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,总反应式为:Zn+H2SO4=ZnSO4+H2↑.乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑,以此进行分析.
解答:
解:A.甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,所以甲中铜片表面有气泡产生,故A错误;
B.乙中不构成原电池,铜片不是电极,故B错误;
C.甲中铜片上氢离子得电子生成氢气,乙中锌和稀硫酸发生置换反应生成氢气,所以两烧杯的溶液中氢离子浓度均减小,溶液的pH值都增大,故C正确;
D.甲能形成原电池,乙不能构成原电池,所以产生气泡的速度甲比乙快,故D错误;
故选C.
B.乙中不构成原电池,铜片不是电极,故B错误;
C.甲中铜片上氢离子得电子生成氢气,乙中锌和稀硫酸发生置换反应生成氢气,所以两烧杯的溶液中氢离子浓度均减小,溶液的pH值都增大,故C正确;
D.甲能形成原电池,乙不能构成原电池,所以产生气泡的速度甲比乙快,故D错误;
故选C.
点评:本题考查了置换反应和原电池的有关知识,题目难度不大,注意把握原电池的组成条件的工作原理.

练习册系列答案
相关题目
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )
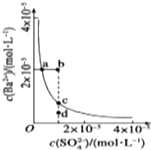

| A、通过加水稀释可以使溶液由b点变到a点 |
| B、加入适量BaCl2(固体) 可以使溶液由d点变到c点 |
| C、d点无BaSO4沉淀生成 |
| D、a点对应的Ksp等于c点对应的Ksp |
已知X、Z、M、W是短周期中的四种元素,且Z、M、W原子序数依次增大,Ne与Wn-的电子数相同.X元素原子形成的离子是一个质子,Z的单质在常温下是无色气体且Z原子的单电子个数是同周期元素原子中最多的.下面有关推测不正确的是( )
| A、ZO3-的空间构型是平面三角形 |
| B、Z、M、W三种元素的第一电离能由大到小的顺序是W>M>Z |
| C、W所在族的氢化物中沸点最低的是HCl |
| D、在ZX4W中,各种粒子间的相互作用力包括极性共价键、配位键、离子键 |
下列物质间,不能发生化学反应的是( )
| A、二氧化硅与生石灰(高温) |
| B、玛瑙与氢氧化钾溶液(常温) |
| C、水晶与碳(高温) |
| D、石英晶体与浓硝酸(常温) |
根据如图结合电化学原理,分析判断下列叙述中不正确的是( )


| A、若向烧杯a中滴加几滴酚酞试液,溶液呈红色 |
| B、装置工作过程中,烧杯b中电极发生氧化反应 |
| C、烧杯c的左侧的电极反应为2H2O+2e-=2OH-+H2↑ |
| D、烧杯c的右侧溶液由黄色变为橙色,是因为该侧电极上发生了反应2CrO42-+H2O-2e-=Cr2O72-+2OH- |
下列有关化学键和化合物的叙述正确的是( )
①共价化合物中只有共价键,离子化合物中一定有离子键
②只含共价键的物质一定是共价化合物
③离子化合物中一定有非金属元素
④离子键和极性键只存在于化合物中
⑤两个非金属原子间不可能形成离子键.
①共价化合物中只有共价键,离子化合物中一定有离子键
②只含共价键的物质一定是共价化合物
③离子化合物中一定有非金属元素
④离子键和极性键只存在于化合物中
⑤两个非金属原子间不可能形成离子键.
| A、①②⑤ | B、②③④ |
| C、①③④⑤ | D、①③⑤ |
淀粉、碘化钾溶液装在羊皮纸袋中,并浸入蒸馏水,过一段时间后取出,用蒸馏水进行实验,(羊皮纸只能让离子通过,高分子不能通过)下列现象证明羊皮纸袋有破损的是( )
| A、使淀粉-KI试纸变蓝色 |
| B、加入KI溶液后变蓝色 |
| C、加入硝酸银溶液产生黄色沉淀 |
| D、加入溴水后液体变蓝色 |
 在容积为2L的密闭容器中,进行如下反应:
在容积为2L的密闭容器中,进行如下反应: