题目内容
下列说法正确的是( )
| A、白磷分子呈正四面体,键角109°28′,1mol白磷含共价键6mol |
| B、石墨晶体呈层状结构,每个碳原子只有3个价电子形成共价键 |
| C、等质量的NO2 和N2O4所含的原子数不相同 |
| D、S8是分子晶体,8个硫原子在同一个平面上,摩尔质量为256g |
考点:判断简单分子或离子的构型,键能、键长、键角及其应用,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A、根据白磷的分子结构图判断;
B、根据石墨的层状结构图分析;
C、先设出物质的质量均为46g,利用n=
来计算和NO2和N2O4的物质的量,结合分子所含有原子数目计算判断;
D、摩尔质量的单位是g/mol.
B、根据石墨的层状结构图分析;
C、先设出物质的质量均为46g,利用n=
| m |
| M |
D、摩尔质量的单位是g/mol.
解答:
解:A、白磷的分子的结构为 ,白磷分子呈正四面体,键角60°,1mol白磷含共价键6mol,故A错误;
,白磷分子呈正四面体,键角60°,1mol白磷含共价键6mol,故A错误;
B、石墨的层状结构图为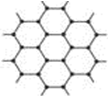 ,每个碳原子与其它3个碳原子形成3个共价键,所以每个碳原子只有3个价电子形成共价键,故B正确;
,每个碳原子与其它3个碳原子形成3个共价键,所以每个碳原子只有3个价电子形成共价键,故B正确;
C、设和NO2和N2O4的质量均为46g,则NO2的物质的量为
=1mol,N2O4的物质的量为
=0.5mol,NO2和N2O4所含原子物质的量之比为1mol×3:0.5mol×6=1:1,则所含的原子数相同,故C错误;
D、S8是分子晶体,8个硫原子不在同一个平面上,摩尔质量为256g/mol,故D错误.
故选B.
 ,白磷分子呈正四面体,键角60°,1mol白磷含共价键6mol,故A错误;
,白磷分子呈正四面体,键角60°,1mol白磷含共价键6mol,故A错误;B、石墨的层状结构图为
 ,每个碳原子与其它3个碳原子形成3个共价键,所以每个碳原子只有3个价电子形成共价键,故B正确;
,每个碳原子与其它3个碳原子形成3个共价键,所以每个碳原子只有3个价电子形成共价键,故B正确;C、设和NO2和N2O4的质量均为46g,则NO2的物质的量为
| 46g |
| 46g/mol |
| 46g |
| 92g/mol |
D、S8是分子晶体,8个硫原子不在同一个平面上,摩尔质量为256g/mol,故D错误.
故选B.
点评:本题考查了分子结构、物质的量的计算、摩尔质量等,题目难度不大,注意把握常见晶体的结构.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
| A、1.6 mol SO2+0.3 mol O2+0.4 mol SO3 |
| B、4.0 mol SO2+2.0 mol O2 |
| C、2.0 mol SO2+1.0 mol O2+2.0 mol SO3 |
| D、3.0 mol SO2+0.5 mol O2+1.0 mol SO3 |
在下列物质中,分别加入金属钠,不能产生氢气的是( )
| A、蒸馏水 | B、煤油 |
| C、无水乙醇 | D、苯酚 |