题目内容
X、Y、Z、W(原子序数依次增大)是元素周期表前四周期中的常见元素,其相关信息如下表:
(1)写出Z2Y2的电子式 ,XY2的结构式 .指出Z的最高价氧化物对应的水化物中的化学键类型 .
(2)X的活泼性比Y的 (填“强”或“弱”);X和Y的气态氢化物中,较稳定的是 (写具体化学式).
(3)下列可以证明Z、W金属性强弱的是 .
A.最高价氧化物对应水化物的溶解性:W<Z B.单质与水反应的剧烈程度:W<Z
C.最高价氧化物对应水化物的碱性:W<Z D.单质与氯气反应中失去的电子数目:Z<W
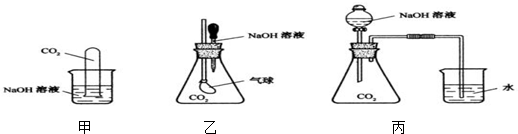
(4)W单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,请写出此反应的化学方程式: .
(5)由氢、X、Y三种原子共同形成多种分子、阴离子,写出其中一种有机分子与一种无机阴离子反应的离子方程式 .
| 元素 | 相关信息 |
| X | X原子的L层电子数是K层电子数的2倍 |
| Y | Y的单质存在Y2、Y3两种同素异形体 |
| Z | Z存在质量数为23,中子数为12的原子核 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X的活泼性比Y的
(3)下列可以证明Z、W金属性强弱的是
A.最高价氧化物对应水化物的溶解性:W<Z B.单质与水反应的剧烈程度:W<Z
C.最高价氧化物对应水化物的碱性:W<Z D.单质与氯气反应中失去的电子数目:Z<W
(4)W单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,请写出此反应的化学方程式:
(5)由氢、X、Y三种原子共同形成多种分子、阴离子,写出其中一种有机分子与一种无机阴离子反应的离子方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W是元素周期表前四周期中的常见元素,X的基态原子L层电子数是K层电子数的2倍,所以X基态原子核外有6个电子,则X是C元素;
Y的单质存在Y2、Y3两种同素异形体,联系O的单质存在O2、O3两种同素异形体,所以Y是O元素;
Z存在质量数为23,中子数为12的核素,则其质子数是11,所以Z是Na元素;
W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色,氢氧化亚铁在空气中会迅速变成灰绿色,最后变成红褐色氢氧化铁,所以W是Fe.
Y的单质存在Y2、Y3两种同素异形体,联系O的单质存在O2、O3两种同素异形体,所以Y是O元素;
Z存在质量数为23,中子数为12的核素,则其质子数是11,所以Z是Na元素;
W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色,氢氧化亚铁在空气中会迅速变成灰绿色,最后变成红褐色氢氧化铁,所以W是Fe.
解答:
解:X、Y、Z、W是元素周期表前四周期中的常见元素,X的基态原子L层电子数是K层电子数的2倍,所以X基态原子核外有6个电子,则X是C元素;
Y的单质存在Y2、Y3两种同素异形体,联系O的单质存在O2、O3两种同素异形体,所以Y是O元素;
Z存在质量数为23,中子数为12的核素,则其质子数是11,所以Z是Na元素;
W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色,氢氧化亚铁在空气中会迅速变成灰绿色,最后变成红褐色氢氧化铁,所以W是Fe,(1)Z是Na,Y是O,过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,电子式为: ,二氧化碳的构型为直线形,即结构式为O=C=O,氢氧化钠是由钠离子和氢氧根构成的离子化合物,故存在离子键和共价键,
,二氧化碳的构型为直线形,即结构式为O=C=O,氢氧化钠是由钠离子和氢氧根构成的离子化合物,故存在离子键和共价键,
故答案为: ;O=C=O;离子键、共价键;
;O=C=O;离子键、共价键;
(2)C的非金属性比O若,故C的氢化物比O的氢化物稳定性若,故答案为:弱;H2O;
(3)A、金属性与金属最高价氧化物的溶解性无关,故A错误;
B、金属越活泼,与水的反应程度越剧烈,故B正确;
C、金属最高价氧化物对应的水化物(即:碱)的碱性越强,金属越活泼,故C正确;
D、活泼性与失去电子数多少无关,故D错误,
故选BC;
(4)铁与高温水蒸气反应生成氢气,反应化学反应方程式为:3Fe+4H2O
Fe3O4+4H2,故答案为:3Fe+4H2O
Fe3O4+4H2;
(5)H、C、O可以构成有机酸:乙酸,能构成含碳的酸式根:碳酸氢根,乙酸与碳酸氢根反应生成二氧化碳气体,故离子反应方程式为:CH3COOH+HCO3-═CH3COO-+H2O+CO2↑,故答案为:CH3COOH+HCO3-═CH3COO-+H2O+CO2↑.
Y的单质存在Y2、Y3两种同素异形体,联系O的单质存在O2、O3两种同素异形体,所以Y是O元素;
Z存在质量数为23,中子数为12的核素,则其质子数是11,所以Z是Na元素;
W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色,氢氧化亚铁在空气中会迅速变成灰绿色,最后变成红褐色氢氧化铁,所以W是Fe,(1)Z是Na,Y是O,过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,电子式为:
 ,二氧化碳的构型为直线形,即结构式为O=C=O,氢氧化钠是由钠离子和氢氧根构成的离子化合物,故存在离子键和共价键,
,二氧化碳的构型为直线形,即结构式为O=C=O,氢氧化钠是由钠离子和氢氧根构成的离子化合物,故存在离子键和共价键,故答案为:
 ;O=C=O;离子键、共价键;
;O=C=O;离子键、共价键;(2)C的非金属性比O若,故C的氢化物比O的氢化物稳定性若,故答案为:弱;H2O;
(3)A、金属性与金属最高价氧化物的溶解性无关,故A错误;
B、金属越活泼,与水的反应程度越剧烈,故B正确;
C、金属最高价氧化物对应的水化物(即:碱)的碱性越强,金属越活泼,故C正确;
D、活泼性与失去电子数多少无关,故D错误,
故选BC;
(4)铁与高温水蒸气反应生成氢气,反应化学反应方程式为:3Fe+4H2O
| ||
| ||
(5)H、C、O可以构成有机酸:乙酸,能构成含碳的酸式根:碳酸氢根,乙酸与碳酸氢根反应生成二氧化碳气体,故离子反应方程式为:CH3COOH+HCO3-═CH3COO-+H2O+CO2↑,故答案为:CH3COOH+HCO3-═CH3COO-+H2O+CO2↑.
点评:本题考查元素的推断,涉及元素位置的判断、氢化物稳定性的判断、离子方程式的书写等知识点,难点是标电子转移的方向和数目,根据元素化合价变化来解答.

练习册系列答案
相关题目
用NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A、11.2LCO和N2混合气体中含有的分子数是0.5NA |
| B、在铁参与的反应中,5.6g铁完全反应失去的电子数一定为0.3NA |
| C、1molNa2O和1molNa2O2中,含阴离子的数目均为NA |
| D、常温下,pH=12的1L氨水中含有的NH3?H2O分子数是0.01NA |
下列条件下,可以大量共存的离子组是( )
| A、某无色溶液中:Na+、Cu2+、Cl-、MnO4- |
| B、含有大量Fe3+的溶液中:Na+、SO42-、K+、SCN- |
| C、含有大量NH4+的溶液中:Ba2+、K+、Cl-、OH- |
| D、在pH=1的溶液中:K+、Fe3+、Cl-、NO3- |
下列有关电解质的说法错误的是( )
| A、强电解质溶液的导电性不一定强于弱电解质溶液的导电性 |
| B、电解质溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数 |
| C、易溶物是强电解质,难溶物一定是弱电解质 |
| D、硫酸钡在水里的溶解度很小,但溶于水的硫酸钡全部电离,所以硫酸钡是强电解质 |
 已知U、V、W、X、Y、Z均为元素周期表中前36号元素,且原子序数依次增大.U、V、W和X、Y分别为同一周期的主族元素,V原子p能级电子总数与s能级电子总数相等.U、Z原子中未成对电子数是同周期中最多的,且基态Z原子核外电子数是基态V原子核外电子数的3倍.X和Y原子的第一至第四电离能如表所示:
已知U、V、W、X、Y、Z均为元素周期表中前36号元素,且原子序数依次增大.U、V、W和X、Y分别为同一周期的主族元素,V原子p能级电子总数与s能级电子总数相等.U、Z原子中未成对电子数是同周期中最多的,且基态Z原子核外电子数是基态V原子核外电子数的3倍.X和Y原子的第一至第四电离能如表所示: