题目内容
18.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )| A. | 达到化学平衡时,v正=v逆=0 | |
| B. | 化学反应速率关系是2v(NH3)=3v(H2O) | |
| C. | 达到化学平衡时,O2的浓度不再改变 | |
| D. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
分析 A.可逆反应属于动态平衡,平衡时正、逆反应速率相等但不为0;
B.速率之比等于化学计量数之比;
C.可逆反应到达平衡时,各组分的浓度保持不变;
D.同种物质的生成速率与消耗速率相等时,可逆反应到达平衡.
解答 解:A.可逆反应属于动态平衡,平衡时同种物质的生成速率与消耗速率相等但不为0,故A错误;
B.速率之比等于化学计量数之比,则3v(NH3)=2v(H2O),故B错误;
C.可逆反应到达平衡时,各组分的浓度保持不变,O2的浓度不再改变,说明反应到达平衡,故C正确;
D.单位时间内生成x mol NO的同时,消耗x mol NH3,均表示正反应速率,反应始终按该比例关系进行,不能说明到达平衡,故D错误,
故选:C.
点评 本题考查化学平衡状态特征、化学平衡状态判断等,注意判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
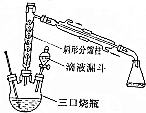
9.乙酸乙酯时重要的工业溶剂,也是生产醋酸纤维、合成药物的原料.实验室制备乙酸乙酯的反应装置示意图和有关数据如下:
实验步骤:
①在三颈烧瓶中,加入10mL乙醇,在振摇下分次加入10mL浓硫酸,混合均匀,加入几粒沸石,按图示装配好各仪器.
②在沙浴小心加热三颈烧瓶,反应温度约为110℃.
③将20mL冰醋酸与20mL乙醇的混合物由液滴漏斗滴入三颈烧瓶中.
④把收集到的溶液用20mL2mol•L-1碳酸钠溶液洗涤2~3次,再用水洗涤.
⑤分液,上面酯层倒入干燥的50mL锥形瓶中,加适量无水硫酸镁,加塞,放置,过滤,得乙酸乙酯粗品.回
答下列问题:
(1)装置中分馏柱的作用是冷凝回流;加入沸石的目的是防止爆沸.
(2)该实验为了提高乙酸的转化率和乙酸乙酯和产率,可采取的措施有使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量等(填字母).
 | 物质 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水的溶解性 |
| 乙醇 | 46 | 0.789 | 78.3 | 溶 | |
| 乙酸 | 60 | 1.050 | 117.9 | 溶 | |
| 乙酸乙酯 | 88 | 0.896 | 77.2 | 不溶 |
①在三颈烧瓶中,加入10mL乙醇,在振摇下分次加入10mL浓硫酸,混合均匀,加入几粒沸石,按图示装配好各仪器.
②在沙浴小心加热三颈烧瓶,反应温度约为110℃.
③将20mL冰醋酸与20mL乙醇的混合物由液滴漏斗滴入三颈烧瓶中.
④把收集到的溶液用20mL2mol•L-1碳酸钠溶液洗涤2~3次,再用水洗涤.
⑤分液,上面酯层倒入干燥的50mL锥形瓶中,加适量无水硫酸镁,加塞,放置,过滤,得乙酸乙酯粗品.回
答下列问题:
(1)装置中分馏柱的作用是冷凝回流;加入沸石的目的是防止爆沸.
(2)该实验为了提高乙酸的转化率和乙酸乙酯和产率,可采取的措施有使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量等(填字母).
6.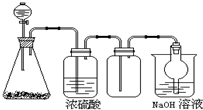 如图是一套实验室制气装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )
如图是一套实验室制气装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )
 如图是一套实验室制气装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )
如图是一套实验室制气装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )| A. | MnO2和浓盐酸 | B. | Na2SO3(s)和浓H2SO4 | ||
| C. | 铁片和浓盐酸 | D. | 电石和水 |
13.下列有关以下物质的工业制法中,正确的是( )
| A. | 制纯碱:往NaOH溶液中 通入少量CO2气体,再蒸发溶液 | |
| B. | 制氯气:以粗盐为原料,经过除杂、浓缩得饱和食盐水,再进行电解所得溶液 | |
| C. | 制镁:用海水为原料,经一系列过程制得氧化镁固体,再用H2还原得镁 | |
| D. | 制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
10.CO(g)+Cl2(g)?COCl2(g)△H<0,当反应达到平衡时,下列措施:①升温、②加压、③增加Cl2的浓度④加催化剂⑤恒压通入惰性气体⑥恒容通入惰性气体.能提高CO转化率的是( )
| A. | ②③ | B. | ③⑤ | C. | ①④ | D. | ③⑥ |
7.分子式为C5H10O3的有机物,在一定条件下能发生如下反应:
①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;
②在一定温度及浓硫酸存在下,能生成一种使溴水褪色的物质;
③在一定温度及浓硫酸存在下,能生成一种分式为C5H8O2的五元环状化合物.
则C5H10O3的结构简式为 ( )
①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;
②在一定温度及浓硫酸存在下,能生成一种使溴水褪色的物质;
③在一定温度及浓硫酸存在下,能生成一种分式为C5H8O2的五元环状化合物.
则C5H10O3的结构简式为 ( )
| A. | HOCH2CH2COOCH2CH3 | B. | HOCH2CH2CH2CH2COOH | ||
| C. | CH3CH2CH(OH)CH2COOH | D. | CH3CH(OH)CH2CH2COOH |
8.有机物M的结构如图所示.关于M的描述正确的是( )
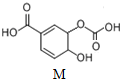

| A. | 分子式为C8H6O6 | |
| B. | 能发生中和、取代、消去、氧化、加成反应 | |
| C. | 1molM与溴水发生反应的产物可能有3种 | |
| D. | 1molM与足量氢氧化钠溶液反应,消耗4molNaOH |
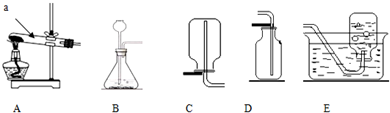
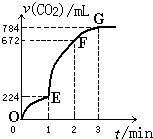 常温下,用纯净的CaCO3与100mL稀盐酸制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况).
常温下,用纯净的CaCO3与100mL稀盐酸制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况).