题目内容
5.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充入C气体,若发生可逆反应C(g)?A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡.下列说法中正确的是( )| A. | 平衡时C的转化率:乙>甲 | B. | 平衡时C的物质的量甲<乙 | ||
| C. | 平均反应速度:乙>甲 | D. | 平衡时A的物质的量甲>乙 |
分析 甲为恒容,乙为恒压,随着反应的进行,甲容器压强逐渐增大,而增大压强,平衡向逆方向移动,而乙容器中压强不变,甲与乙容器相比,甲中反应速率较大、平衡向着逆向移动,以此解答该题.
解答 解:甲为恒容,乙为恒压,随着反应的进行,甲容器压强逐渐增大,而乙压强不变,
A.增大压强平衡向逆方向移动,C的转化率减小,则平衡时C的转化率:乙>甲,故A正确;
B.增大压强平衡向逆方向移动,平衡时C的物质的量:甲>乙,故B错误;
C.压强越大反应速率越大,则反应速率:甲>乙,故C错误;
D.增大压强平衡向逆方向移动,则平衡时A的物质的量:乙>甲,故D错误.
故选A.
点评 本题考查化学平衡及其影响因素,为高频考点,题目难度不大,本题注意从压强对平衡移动的影响的角度比较甲乙两个状态,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.在CaCl2、MgI2、K2CO3、HClO、NaOH这几种物质中,含有共价键的离子化合物有( )
| A. | 1种 | B. | 3种 | C. | 2种 | D. | 4种 |
10.下列实验操作能达到实验目的是( )
| A. | 用向上排空气法收集Na2SO3与浓硫酸反应生成SO2 | |
| B. | 用50mL量筒准确量取25.00mL NaOH溶液 | |
| C. | 除去乙酸乙酯中溶解解的乙酸,加NaOH溶液充分振荡、分液 | |
| D. | 向含有CuCl2的FeC13溶液中加足量铁粉搅拌、过滤,得到纯净FeCl3溶液. |
17.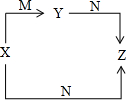 X.Y、Z、M、N五种物质中,X、Y、Z中均含有钠元素,X和M都是常见的单质,N是水,它们之间具有如图所示的转化关系.下列有关物质的推断不正确的是( )
X.Y、Z、M、N五种物质中,X、Y、Z中均含有钠元素,X和M都是常见的单质,N是水,它们之间具有如图所示的转化关系.下列有关物质的推断不正确的是( )
 X.Y、Z、M、N五种物质中,X、Y、Z中均含有钠元素,X和M都是常见的单质,N是水,它们之间具有如图所示的转化关系.下列有关物质的推断不正确的是( )
X.Y、Z、M、N五种物质中,X、Y、Z中均含有钠元素,X和M都是常见的单质,N是水,它们之间具有如图所示的转化关系.下列有关物质的推断不正确的是( )| A. | X只是钠 | B. | Y只是Na2O | C. | Z只是NaOH | D. | M可能是O2 |
17.以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1
①该反应在常温下不能自发进行(填“能”与“不能”);
②一定温度和压强下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是bd(填序号)
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2mol H-O
c.c(CO)=c(H2) d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表两组数据:
①该反应为放(填“吸”或“放”)热反应;
②已知800℃时,上述反应的平衡常数K=1.若用2molCO和5mol H2O相互混合并加热到800℃,反应达到平衡时下列说法正确的是B(填序号)
A.此时水的转化率为71.4%
B.此时CO2的体积分数为20.4%
C.若再向容器内通入5mol H2O,则达到新平衡时,H2O的转化率升高
D.若从容器内移走5mol H2O,则达到新平衡时,CO的转化率升高.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1
①该反应在常温下不能自发进行(填“能”与“不能”);
②一定温度和压强下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是bd(填序号)
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2mol H-O
c.c(CO)=c(H2) d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表两组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| CO | H2O | H2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 3 |
②已知800℃时,上述反应的平衡常数K=1.若用2molCO和5mol H2O相互混合并加热到800℃,反应达到平衡时下列说法正确的是B(填序号)
A.此时水的转化率为71.4%
B.此时CO2的体积分数为20.4%
C.若再向容器内通入5mol H2O,则达到新平衡时,H2O的转化率升高
D.若从容器内移走5mol H2O,则达到新平衡时,CO的转化率升高.
14.元素周期律和元素周期表是学习化学的重要工具,下列说法不正确的是( )
| A. | HF、HCl、HBr、HI的还原性依次增强,热稳定性依次减弱 | |
| B. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| C. | ⅠA金属元素是同周期中金属性最强的元素 | |
| D. | P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 |
15.H、D、T、H+可以表示( )
| A. | 四种不同元素 | B. | 化学性质不同的氢原子 | ||
| C. | 氢元素的四种同位素 | D. | 氢元素的四种不同微粒 |
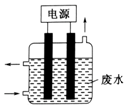 “8•12”天津港危化仓库爆炸,造成生命、财产的特大损失.据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN).请回答下列问题:
“8•12”天津港危化仓库爆炸,造成生命、财产的特大损失.据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN).请回答下列问题: .
.