题目内容
设NA为阿伏加德罗常数的数值.下列说法错误的是( )
| A、20g重水(D2O)中含有10NA个电子 |
| B、标准状况下,22.4L一氯甲烷的分子数约为NA |
| C、4.6g Na在氧气中完全反应生成Na2O和Na2O2,转移电子数为0.2NA |
| D、25℃时,1L pH=14的Ba(OH)2溶液中,Ba2+数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据重水的质量计算出物质的量及含有的电子数;
B、根据标况下一氯甲烷的体积计算出物质的量及数目;
C、根据钠的质量计算出物质的量,再根据电子守恒计算出转移的电子数;
D、根据溶液的pH及溶液的体积计算出氢氧根离子的物质的量及钡离子的物质的量和数目.
B、根据标况下一氯甲烷的体积计算出物质的量及数目;
C、根据钠的质量计算出物质的量,再根据电子守恒计算出转移的电子数;
D、根据溶液的pH及溶液的体积计算出氢氧根离子的物质的量及钡离子的物质的量和数目.
解答:
解:A、20g重水的物质的量为1mol,含有10mol电子,含有10NA个电子,故A正确;
B、标况下,22.4L一氯甲烷的物质的量为1mol,含有一氯甲烷的分子数约为NA,故B正确;
C、4.6g钠的物质的量为0.2mol,完全反应失去0.2mol电子,转移电子数为0.2NA,故C正确;
D、25℃时,1L pH=14的Ba(OH)2溶液中,氢氧根离子的浓度为1mol/L,氢氧根离子的物质的量为1mol,含有钡离子的物质的量为0.5mol,Ba2+数为0.5NA,故D错误;
故选:D.
B、标况下,22.4L一氯甲烷的物质的量为1mol,含有一氯甲烷的分子数约为NA,故B正确;
C、4.6g钠的物质的量为0.2mol,完全反应失去0.2mol电子,转移电子数为0.2NA,故C正确;
D、25℃时,1L pH=14的Ba(OH)2溶液中,氢氧根离子的浓度为1mol/L,氢氧根离子的物质的量为1mol,含有钡离子的物质的量为0.5mol,Ba2+数为0.5NA,故D错误;
故选:D.
点评:本题考查了阿伏伽德罗常数,注意标准状况下条件及物质的状态,注意电子守恒的应用,本题难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实现下列转化,必须加入氧化剂或还原剂的是( )
| A、Cl2→HClO+HCl |
| B、NH4+→NH3 |
| C、NH3→NO |
| D、P2O5→H3PO4 |
下列有关四种基本反应类型与氧化还原反应关系的说法中正确的是( )
| A、化合反应一定是氧化还原反应 |
| B、分解反应一定不是氧化还原反应 |
| C、置换反应一定是氧化还原反应 |
| D、复分解反应不一定是氧化还原反应 |
已知人造羊毛的结构为 ,则合成人造羊毛的单体是( )
,则合成人造羊毛的单体是( )
①CH2=CHCN ②CH2=CHCOOCH3 ③CH2=C(CN)CH3 ④CH3COOCH=CH2⑤CH3COOH ⑥CH2=C(CN)CH=CHOH.
 ,则合成人造羊毛的单体是( )
,则合成人造羊毛的单体是( )①CH2=CHCN ②CH2=CHCOOCH3 ③CH2=C(CN)CH3 ④CH3COOCH=CH2⑤CH3COOH ⑥CH2=C(CN)CH=CHOH.
| A、①② | B、⑤⑥ | C、③④ | D、①④ |
下列叙述正确的是( )
| A、水的摩尔质量是18g |
| B、HCl的摩尔质量等于NA个HCl分子的质量 |
| C、摩尔是七个基本物理量之一 |
| D、1mol CO2的质量以克为单位时,在数值上等于CO2的相对分子质量 |
下列各种说法中正确的是( )
| A、极性键只能形成极性分子 |
| B、CO2中碳原子是sp2杂化 |
| C、形成配位键的条件是一方有空轨道,另一方有孤对电子 |
| D、共价键形成的条件是成键原子必须有未成对电子 |
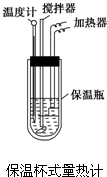 在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.