题目内容
4.在Na2O2与CO2的反应中,下列说法正确的是( )| A. | 该反应中Na2O2是氧化剂,CO2是还原剂 | |
| B. | 1mol Na2O2参加反应,有2mole-转移 | |
| C. | Na2O2晶体中阴阳离子个数比为1:1 | |
| D. | Na2O2晶体中含有离子键和共价键 |
分析 Na2O2晶体中阴阳离子个数比为1:2,该反应中,O元素化合价由-1价分别变为-2价和0价,所以过氧化钠既是氧化剂又是还原剂,以此解答该题.
解答 解:A.该反应中,O元素化合价由-1价变为-2价和0价,所以过氧化钠既是氧化剂又是还原剂,故A错误;
B.若有2 mol Na2O2参加反应,则转移电子的物质的量为2mol×(1-0)=2 mol,则1molNa2O2完全反应时转移电子1mole-,故B错误;
C.过氧化钠中过氧根离子显-2价,其电子式是 ,晶体中阴阳离子个数比为1:2,故C错误;
,晶体中阴阳离子个数比为1:2,故C错误;
D.过氧化钠为离子化合物,含有离子键和共价键,故D正确.
故选D.
点评 本题考查氧化还原反应以及过氧化钠知识,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量是14.4g,若其中水的质量是7.2g,则CO的质量是( )
| A. | 2.8g | B. | 4.4g | ||
| C. | 5.6g | D. | 在2.8g和5.6g之间 |
9.拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图.下列对该化合物叙述不正确的是( )


| A. | 属于芳香化合物 | B. | 具有酯类化合物的性质 | ||
| C. | 属于烃 | D. | 在一定条件下可以发生加成反应 |
16. 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )| A. | 莽草酸的分子之间可能发生酯化反应 | |
| B. | 莽草酸的分子式为C7H4O5 | |
| C. | 莽草酸中含有苯环 | |
| D. | 莽草酸不能使溴水褪色 |
14.下列说法正确的是( )
| A. | 用含有铁粉的透气小袋与食品一起密封包装,铁粉是常用的脱氧剂 | |
| B. | 浓硫酸可以盛放在铝桶中,说明铝不能与浓硫酸反应 | |
| C. | 过滤用到的玻璃仪器有铁架台、烧杯、漏斗、玻璃棒、滤纸 | |
| D. | 用氢氟酸雕刻玻璃,说明氢氟酸是强酸 |
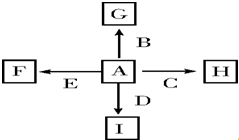 图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.
图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物. 可简写为
可简写为  .降冰片烯的分子结构可表示为
.降冰片烯的分子结构可表示为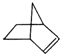
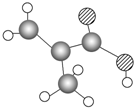 某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键). .
.