题目内容
下列说法不正确的是( )
| A、陶瓷是以黏土和石灰石为原料,经高温烧结而成的 |
| B、高纯单质硅可以制成光电池,将光能直接转换为电能 |
| C、水玻璃可作木材的防火剂 |
| D、向饱和Na2SiO3溶液中通入足量CO2,然后蒸发结晶,最后灼烧,得到Na2CO3、SiO2 |
考点:硅和二氧化硅
专题:碳族元素
分析:A.黏土经过高温烧结可以获得陶瓷;
B.单质硅导电性介于导体与绝缘体之间;
C.硅酸钠耐高温;
D.硅酸的酸性弱于碳酸,碳酸钠与二氧化硅 高温条件反应生成硅酸钠.
B.单质硅导电性介于导体与绝缘体之间;
C.硅酸钠耐高温;
D.硅酸的酸性弱于碳酸,碳酸钠与二氧化硅 高温条件反应生成硅酸钠.
解答:
解:A.陶瓷黏土经过高温烧结而成,故A错误;
B.单质硅导电性介于导体与绝缘体之间,是良好的半导体,可以制成光电池,将光能直接转换为电能,故B正确;
C.水玻璃的主要成分为硅酸钠,硅酸钠耐高温,不易燃烧,故C正确;
D.向饱和Na2SiO3溶液中通入足量CO2,然后蒸发结晶,最后灼烧,得到硅酸钠,故D错误;
故选:AD.
B.单质硅导电性介于导体与绝缘体之间,是良好的半导体,可以制成光电池,将光能直接转换为电能,故B正确;
C.水玻璃的主要成分为硅酸钠,硅酸钠耐高温,不易燃烧,故C正确;
D.向饱和Na2SiO3溶液中通入足量CO2,然后蒸发结晶,最后灼烧,得到硅酸钠,故D错误;
故选:AD.
点评:本题考查了硅及其化合物的性质和用途,性质决定用途,明确硅及其化合物性质是解题关键,注意相关知识的积累.

练习册系列答案
相关题目
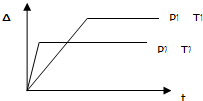 有一化学平衡:mA(气)+nB(气)?pC(气)+qD(气),如图表示A的
有一化学平衡:mA(气)+nB(气)?pC(气)+qD(气),如图表示A的转化率同温度、压强的关系,分析此图可以得出的正确结论是( )
| A、正反应是吸热反应,m+n>p+q |
| B、正反应是吸热反应,m+n<p+q |
| C、正反应是放热反应,m+n>p+q |
| D、正反应是放热反应,m+n<p+q |
下列说法正确的是( )
| A、苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
| B、元素分析仪可以同时对碳、氢、氧、硫等多种元素进行分析 |
| C、乙醇、乙酸均能与金属钠反应产生氢气,是因为它们所含的官能团相同 |
| D、糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同 |
以下说法:①冰、水混合物属于纯净物②纯碱晶体和胆矾均是盐③硫酸、干冰既是纯净物又是化合物④雾与空气均属于混合物⑤盐酸和食醋既是化合物又是酸.其中正确的是( )
| A、①②③④ | B、②⑤ |
| C、③⑤ | D、①③④ |
下列各组物质中,属于同分异构体的是( )
| A、CH3CHCH2CH2CH3CH3和CH3CHCH2CH2CH2CH3CH3 |
| B、H2N-CH2-COOH和H3C-CH2-NO2 |
| C、CH3-CH2-CH2-COOH和H3C-CH2-CH2-CH2-COOH |
| D、H3C-CH2-O-CH2-CH3和CH3CHCH3CH3 |
在含有1mol HNO3和2molH2SO4的混合稀溶液中,加入1.5molCu,加热充分反应,产生的气体在标准状况下的体积约为( )
| A、5.6L | B、11.2L |
| C、22.4L | D、44.8L |
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、pH=1的溶液中:Na+、K+、MnO4-、CO32-、 |
| B、c(H+)=1×10-13 mol?L-1的溶液中:Mg2+、Cu2+、NO3- |
| C、0.1 mol?L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- |
| D、0.1 mol?L-1FeCl3溶液中:Fe2+、SCN-、SO42- |
运用有关概念判断下列叙述正确的是( )
| A、1mol H2燃烧放出的热量为H2的燃烧热 |
| B、Na2SO3和H2O2的反应为氧化还原反应 |
C、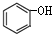 和 和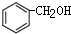 互为同系物 互为同系物 |
| D、BaSO4的水溶液不导电,故BaSO4是弱电解质 |
下列各组物质中,均为纯净物的一组是( )
| A、碘酒 干冰 |
| B、液氯 浓硫酸 |
| C、石灰石 氨水 |
| D、CuSO4?5H2O 冰水混合物 |