题目内容
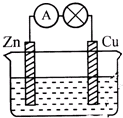 用铜片、锌片和200mL稀H2SO4等组成原电池(如图).若整个实验过程有6.5g锌溶解,此时H2SO4恰好全部用完.回答下列问题:
用铜片、锌片和200mL稀H2SO4等组成原电池(如图).若整个实验过程有6.5g锌溶解,此时H2SO4恰好全部用完.回答下列问题:(1)写出正极的电极反应式
(2)试计算:铜片上共放出
分析:(1)铜、锌和稀硫酸构成的原电池中,锌易失电子而作负极,铜作正极,正极上氢离子得电子生成氢气;
(2)根据锌和氢气之间的关系计算氢气的体积、锌和转移电子之间的关系式计算转移电子的物质的量,根据锌和硫酸之间的关系计算硫酸的物质的量,再结合物质的量浓度公式计算硫酸的浓度.
(2)根据锌和氢气之间的关系计算氢气的体积、锌和转移电子之间的关系式计算转移电子的物质的量,根据锌和硫酸之间的关系计算硫酸的物质的量,再结合物质的量浓度公式计算硫酸的浓度.
解答:解:(1)该原电池中,锌作负极,铜作正极,正极上氢离子得电子生成氢气,电极反应式为:2H++2e-═H2↑,所以看到的现象是:有大量气体生成,负极上电极反应式为:Zn-2e-═Zn2+,
故答案为:2H++2e-═H2↑;有大量气体生成;Zn-2e-═Zn2+;
(2)该原电池中电池反应式为2H++Zn=H2↑+Zn2+,根据锌和氢气之间的关系式得氢气的体积=
×1×22.4L/mol=2.24L,根据Zn-2e-═Zn2+中锌和转移电子之间的关系式得,转移电子的物质的量=
×2=0.2mol,根据H2SO4+Zn=H2↑+ZnSO4中锌和硫酸的关系式得,硫酸的物质的量=
×1=0.1mol,硫酸的物质的量浓度=
=0.5mol/L,
故答案为:2.24;0.2;0.5.
故答案为:2H++2e-═H2↑;有大量气体生成;Zn-2e-═Zn2+;
(2)该原电池中电池反应式为2H++Zn=H2↑+Zn2+,根据锌和氢气之间的关系式得氢气的体积=
| ||
| 1 |
| ||
| 1 |
| ||
| 1 |
| 0.1mol |
| 0.2L |
故答案为:2.24;0.2;0.5.
点评:本题考查了原电池原理、物质的量的计算等知识点,明确电极上电极反应、物质之间的关系即可解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目