题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、17g-OH(羟基)所含电子总数为9NA |
| B、标准状况下,22.4LCHCl3中所含分子数为NA |
C、32g S8单质(结构如图)中含有的S-S键个数为2NA |
| D、18gD2O中含有的原子数为3NA |
考点:阿伏加德罗常数
专题:
分析:A.1个羟基含有9个电子;
B.气体摩尔体积只适用于气体;
C.一个S8分子(其“皇冠”结构如图)中含有的S-S键个数为8个;
D.质量换算物质的量结合分子式计算.
B.气体摩尔体积只适用于气体;
C.一个S8分子(其“皇冠”结构如图)中含有的S-S键个数为8个;
D.质量换算物质的量结合分子式计算.
解答:
解:A.1个羟基含有9个电子,17g-OH(羟基)的物质的量=
=1mol,含电子总数为9NA,故A正确;
B.标准状况下CHCl3为液体,不能使用气体摩尔体积,故B错误;
C.一个S8分子(其“皇冠”结构如图)中含有的S-S键个数为8个,32gS8单质物质的量=
=0.125mol,含有的S-S键个数为NA,故C错误;
D.18gD2O所含的原子数=
×3NA=2.7NA,故D错误;
故选:A.
| 17g |
| 17g/mol |
B.标准状况下CHCl3为液体,不能使用气体摩尔体积,故B错误;
C.一个S8分子(其“皇冠”结构如图)中含有的S-S键个数为8个,32gS8单质物质的量=
| 32g |
| 8×32g/mol |
D.18gD2O所含的原子数=
| 18g |
| 20g/mol |
故选:A.
点评:本题考查阿伏伽德罗常数的应用,掌握阿伏伽德罗常数与物质的量、摩尔质量等物理量之间的转化,注意气体摩尔体积的条件应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化合物A的分子式为C4H9NO2,A的同分异构体中属于氨基酸的有( )
| A、5种 | B、4种 | C、3种 | D、6种 |
下列说法中,正确的是( )
| A、从碘水中提取碘单质,可选用酒精作有机萃取剂 |
| B、蒸馏操作时,应使温度计的水银球深入液体中 |
| C、与盐酸反应生成CO2,碳酸钠比碳酸氢钠快 |
| D、向Na2CO3和NaHCO3溶液中分别滴加酚酞试液,两者都显红色 |
在t℃时,某NaOH稀溶液中,c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=13,则在该温度下,将100mL 0.10mol/L的稀硫酸与100mL 0.40mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)( )
| A、11.52 |
| B、11.70 |
| C、11.82 |
| D、12.00 |
建构数学模型来研究化学问题,既直观又简洁.下列建构的数轴模型正确的是( )
A、钠在氧气中燃烧,钠的氧化产物: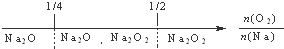 |
B、铁在Cl2中燃烧,铁的氧化产物: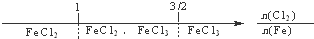 |
C、NH3与Cl2反应,反应产物: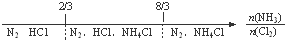 |
D、FeBr2溶液中通入Cl2,铁元素存在形式: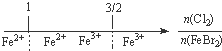 |
下列有关说法,不正确的是( )
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②向煤中加入适量石灰石,在煤燃烧时最终生成CaSO4,可减少SO2对大气的污染
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤为证明NaHCO3溶液中混有Na2CO3,取少量溶液,加入澄清石灰水,若有白色沉淀生成,则证明混有Na2CO3.
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②向煤中加入适量石灰石,在煤燃烧时最终生成CaSO4,可减少SO2对大气的污染
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤为证明NaHCO3溶液中混有Na2CO3,取少量溶液,加入澄清石灰水,若有白色沉淀生成,则证明混有Na2CO3.
| A、仅①③④⑤ | B、仅②③④ |
| C、仅①③④ | D、仅①②④⑤ |
下列现象或新技术的应用中,不涉及胶体性质的是( )
| A、在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 |
| B、使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 |
| C、清晨,在茂密的树林中,常常可以看到枝叶间透过的一道道光线 |
| D、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.