题目内容
1.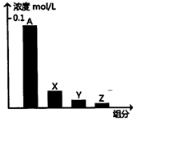 常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )| A. | A可能表示Na+ | |
| B. | A可能表示乙酸分子 | |
| C. | 若图中A表示CH3COO-,可以证明乙酸是弱酸 | |
| D. | 该混合溶液中:c(A)+c(Y)=c(X)+c(Z) |
分析 常温下,0.2mol/L的乙酸与等浓度的NaOH溶液等体积混合后,反应后溶质为醋酸钠,CH3COO-部分水解,溶液呈碱性,则反应后溶液中满足:c(Na+)=0.1mol/L>c(CH3COO-)>c(OH-)>c(CH3COOH)>c(H+),结合图象可知A为CH3COO-、X为OH-、Y为CH3COOH、Z为H+,据此进行解答.
解答 解:反应后溶质为CH3COONa,CH3COO-部分水解,溶液呈碱性,则反应后溶液中满足:c(Na+)=0.1mol/L>c(CH3COO-)>c(OH-)>c(CH3COOH)>c(H+),结合图象可知A为CH3COO-、X为OH-、Y为CH3COOH、Z为H+,
A.根据分析可知,A为CH3COO-,故A错误;
B.A为CH3COO-,A不可能为A为CH3COOH,故B错误;
C.A表示CH3COO-,表明醋酸根离子部分水解,可证明醋酸为弱酸,故C正确;
D.A为CH3COO-、X为OH-、Y为CH3COOH、Z为H+,则c(A)+c(Y)=c(X)+c(Z)为:c(CH3COO-)+c(CH3COOH)=c(OH-)+c(H+),由于醋酸根离子的水解程度较小,则c(CH3COO-)>c(OH-)+c(H+),故D错误;
故选C.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,正确推断各粒子组成为解答关键,注意掌握离子浓度大小比较方法,试题有利于提高学生的分析能力及逻辑推理能力.

练习册系列答案
相关题目
10.化学与社会、生产、生活和科技都密切相关.下列说法正确的是( )
| A. | 军舰船底镶嵌锌块作正极,以防船体被腐蚀 | |
| B. | “天宫二号”使用的碳纤维,是一种新型有机高分子材料 | |
| C. | 烈性炸药硝化甘油是由甘油(丙三醇)硝化制得,它属于酯类 | |
| D. | 蚊虫叮咬时释放出的蚁酸使人觉得不适,可以用肥皂水氧化蚁酸处理 |
11.在铁的氧化物和氧化铝组成的混合物中,加入 2mol/L 硫酸溶液 65mL,恰好完全反应,所得溶液中Fe2+能被标准状况下 112mL 氯气氧化.则原混合物中金属元素和氧元素的原子个数之比为( )
| A. | 9:13 | B. | 5:7 | C. | 4:3 | D. | 3:4 |
9.已知:将Cl2通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值与温度高低有关,当n(NaOH)=a mol时,下列有关说法错误的是( )
| A. | 参加反应的氯气的物质的量等于$\frac{1}{2}$amol | |
| B. | 改变温度,产物中NaClO3的最大理论产量为$\frac{1}{7}$amol | |
| C. | 改变温度,反应中转移电子的物质的量n的范围:$\frac{1}{2}$amol≤n≤$\frac{5}{6}$amol | |
| D. | 某温度下,若反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(C{l}^{-})}{c(Cl{O}_{3}^{-})}$=$\frac{11}{2}$ |
6.下列说法不正确的是( )
| A. | 0.02 mol•L-1醋酸与0.02 mol•L-1NaOH等体积混合后的溶液中加少量的CH3COONa固体,则$\frac{c(C{H}_{3}CO{O}^{-})}{C(N{a}^{+})}$ 增大 | |
| B. | t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2,$\frac{c(NO)•c(S{O}_{3})}{c(N{O}_{2})•c(S{O}_{2})}$ 的值及SO2转化率不变 | |
| C. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 | |
| D. | lmol该化合物( 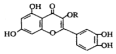 )与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、8mol )与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、8mol |
13.下列有关苯乙烯( 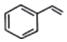 )的说法错误的是( )
)的说法错误的是( )
 )的说法错误的是( )
)的说法错误的是( )| A. | 苯乙烯与乙烯互为同系物 | B. | 所有原子可能在同一平面 | ||
| C. | 可使酸性KMnO4溶液褪色 | D. | 可发生加成反应 |
10.某同学用Na2CO3和NaHCO3溶液进行如图所示实验.下列说法中,正确的是( )


| A. | 实验前两溶液的pH相等 | |
| B. | 实验前两溶液中离子种类完全相同 | |
| C. | 加入CaCl2溶液后生成的沉淀一样多 | |
| D. | 加入CaCl2溶液后反应的离子方程式都是CO32-+Ca2+═CaCO3↓ |
11.下列说法中不正确的是( )
| A. | pH=a的氨水溶液,稀释10倍后,其pH=b,则b<a-1 | |
| B. | pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液中c(Na+):③<②<① | |
| C. | 某温度Ksp(Ag2S)=6×10-50,Ksp(AgCl)=2×10-6,则 2AgCl(s)+S2-(aq)?Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×1037 | |
| D. | 一定浓度的 NaHS 溶液中:c(Na+)+c(OH-)═c(H+)+c(HS-)+2c(H2S) |