题目内容
将4gNaOH固体溶于水配成250mL溶液,此溶液中NaOH的物质的量浓度为 mol/L.取出10mL此溶液,其中含有NaOH g.将取出的溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为 mol/L.
考点:物质的量浓度的相关计算
专题:计算题
分析:根据n=
计算氢氧化钠的物质的量,再根据c=
计算溶液物质的量浓度,溶液是均匀的,取出10mL溶液的浓度与原溶液浓度相等,根据n=cV计算取出10mL溶液中氢氧化钠的物质的量,再根据m=nM计算氢氧化钠的质量,根据c=
计算稀释后溶液物质的量浓度.
| m |
| M |
| n |
| V |
| n |
| V |
解答:
解:4g NaOH的物质的量为
=0.1mol,溶于水配成250mL溶液,此溶液中NaOH的物质的量浓度为
=0.4mol/L,溶液是均匀的,取出10mL溶液的浓度与原溶液浓度相等,取出10mL溶液中NaOH的物质的量=0.01L×0.4mol/L=0.004mol,10mL溶液中氢氧化钠的质量=0.004mol×40g/mol=0.16g,将该10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为
=0.04mol/L,
故答案为:0.4;0.16;0.04.
| 4g |
| 40g/mol |
| 0.1mol |
| 0.25L |
| 0.004mol |
| 0.1L |
故答案为:0.4;0.16;0.04.
点评:本题考查物质的量浓度有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在试管的内壁附着下列物质,用稀盐酸浸泡而不能除去的是( )
| A、用足量一氧化碳还原氧化铁后留下的物质 |
| B、用足量氢气还原氧化铜后留下的红色物质 |
| C、盛石灰水后留下的白色固体 |
| D、硫酸铁溶液与氢氧化钠溶液反应后留下的红褐色固体 |
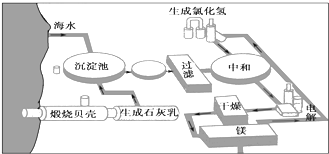 如图是工业上生产镁的流程.
如图是工业上生产镁的流程.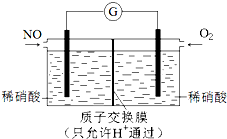 NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
 (1)在原电池中,通常较活泼的金属做
(1)在原电池中,通常较活泼的金属做